
А. В. Перышкин
(2013)
Учебник для общеобразовательных учреждений
УДК 373.167.1:53 ББК 22.3я72 П27
Перышкин, А. В. Физика. 8 кл.: учеб. для общеобразоват. учреждений / А. В. Перышкин. — М. : Дрофа, 2013. — 237, [3] с. : ил. ISBN 978-5-358-09884-8
ГЛАВА 1. Тепловые явления
В окружающем нас мире происходят различные физические явления, которые связаны с нагреванием и охлаждением тел. Мы знаем, что при нагревании холодная вода вначале становится тёплой, а затем горячей.
Такими словами, как «холодный», «тёплый» и «горячий», мы указываем на различную степень нагретости тел, или, как говорят в физике, на различную температуру тел. Температура горячей воды выше температуры холодной. Температура воздуха летом выше, чем зимой.
Температуру тел измеряют с помощью термометра и выражают в градусах Цельсия (°С).
Вам уже известно, что диффузия при более высокой температуре происходит быстрее. Это означает, что скорость движения молекул и температура связаны между собой. При повышении температуры скорость движения молекул увеличивается, при понижении — уменьшается.
Следовательно, температура тела зависит от скорости движения молекул.
Тёплая вода состоит из таких же молекул, как и холодная. Разница между ними заключается лишь в скорости движения молекул.
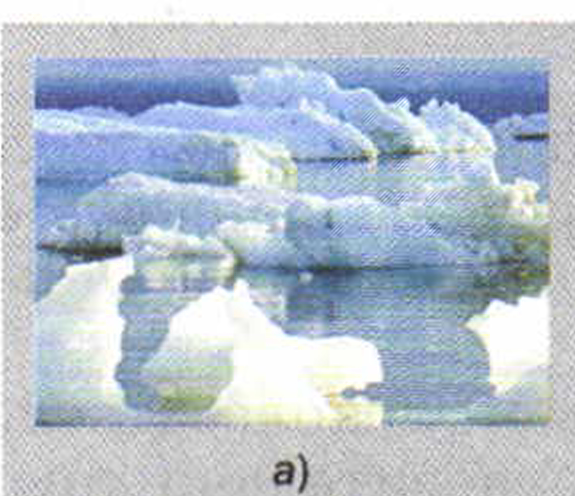
Явления, связанные с нагреванием или охлаждением тел, с изменением температуры, называются тепловыми. К таким явлениям относятся, например, нагревание и охлаждение воздуха, таяние льда, плавление металлов и др.


Примеры тепловых явлений: а — таяние льда; б — замерзание воды

Молекулы или атомы, из которых состоят тела, находятся в непрерывном беспорядочном движении. Их количество в окружающих нас телах очень велико. Так, в объёме, равном 1 см3 воды, содержится около 3,34 • 1022 молекул. Каждая молекула движется по очень сложной траектории. Это связано с тем, что, например, частицы газа, движущиеся с большими скоростями в разных направлениях, сталкиваются друг с другом и со стенками сосуда. В результате этого они изменяют свою скорость и снова продолжают движение. На рис. 1 изображены траектории движения микроскопических частиц краски, растворённой в воде.
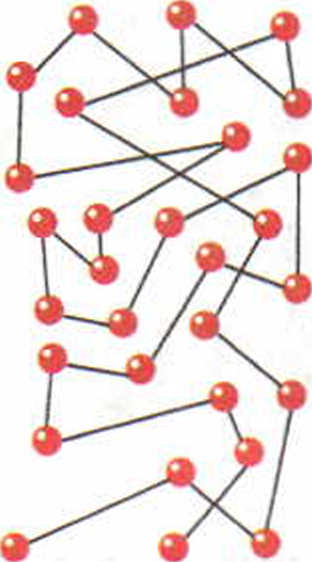
Рис. 1. Траектория движения микрочастиц краски, растворённой в воде

Модель кристаллической решётки льда
Поскольку со скоростью движения молекул тела связана его температура, беспорядочное движение частиц называют тепловым движением.
В жидкостях молекулы могут колебаться, вращаться и перемещаться относительно друг друга. В твёрдых телах молекулы и атомы колеблются около некоторых средних положений.
В тепловом движении участвуют все молекулы тела, поэтому с изменением характера теплового движения изменяется и состояние тела, его свойства. Так, при повышении температуры лёд начинает таять, превращаясь в жидкость. Если понижать температуру, например, ртути, то она из жидкости превращается в твёрдое тело.

Плавление металла
При изучении физики рассматриваются механические, тепловые, световые, электрические и другие явления. С некоторыми механическими явлениями мы уже познакомились. Известно также, что существует два вида механической энергии: кинетическая и потенциальная.
Всякое движущееся тело обладает кинетической энергией. Так, например, кинетической энергией обладает летящая птица, движущиеся самолёт, мяч, текущая вода и т. д. Кинетическая энергия тела зависит от его массы и от скорости движения тела.
Потенциальная энергия определяется взаимным положением взаимодействующих тел или его отдельных частей. Например, потенциальной энергией обладают поднятый над землёй камень, сжатая или растянутая пружина и т. д.
Кинетическая и потенциальная энергия — это два вида механической энергии, они могут превращаться друг в друга.
Как же происходит превращение одного вида энергии в другой?
Свинцовый шар, лежащий на свинцовой плите, поднимем вверх и отпустим (рис. 2, а). При падении скорость шара увеличивается, а высота подъёма уменьшается. Следовательно, его кинетическая энергия возрастает, а потенциальная уменьшается. Это значит, что происходит превращение потенциальной энергии шара в кинетическую. После того как шар ударится о свинцовую плиту, он остановится (рис. 2, б). Его кинетическая и потенциальная энергия будут равны нулю.


Тела, обладающие кинетической энергией: а — летящая птица; б — движущийся самолёт

1. Какие тепловые явления вы знаете?
2. Что характеризует температура?
3. Как связана температура тела со скоростью движения его молекул?
4. Чем отличается движение молекул в газах, жидкостях и твёрдых телах?
Температура тела находится в тесной связи со средней кинетической энергией молекул. Чем выше температура тела, тем больше средняя кинетическая энергия его молекул. При понижении температуры тела средняя кинетическая энергия его молекул уменьшается.

Тела, обладающие потенциальной энергией: а—деформированная пружина: б — камень, поднятый над Землёй
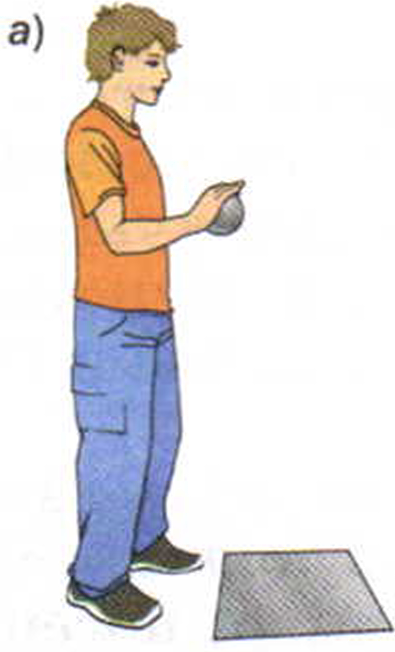
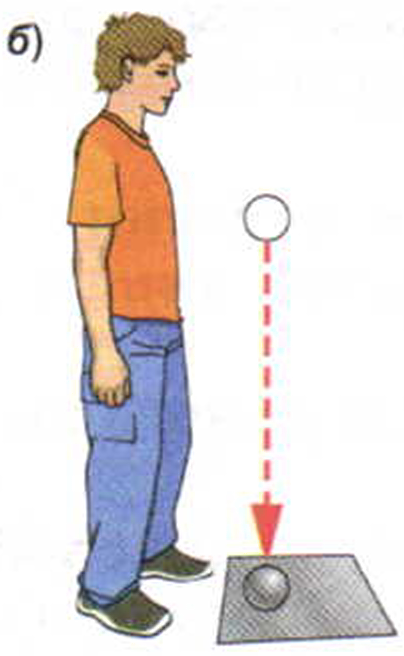
Рис. 2. Превращение механической энергии свинцового шара
Значит ли это, что механическая энергия, которой обладал шар, бесследно исчезла? По-видимому, нет.
Механическая энергия превратилась в другую форму энергии. Что же представляет собой эта другая форма энергии? Рассмотрим шар и плиту после удара. Оказывается, что шар немного сплюснулся, а на плите возникла небольшая вмятина. Шар и плита при ударе деформировались. Измерим температуру шара и плиты сразу после удара. Мы заметим, что они нагрелись.
Таким образом, в результате удара шара о плиту изменилось состояние этих тел — они деформировались и нагрелись. Но если изменилось состояние тел, то изменилась и энергия частиц, из которых состоят тела. Действительно, мы знаем, что при нагревании тела увеличивается средняя скорость движения молекул. Значит, увеличивается их средняя кинетическая энергия. Молекулы обладают также и потенциальной энергией. Ведь они взаимодействуют друг с другом: притягиваются, а при дальнейшем сближении — отталкиваются. Когда тело деформировалось, то изменилось взаимное расположение его молекул, а значит, изменилась и их потенциальная энергия.
Итак, при соударении изменилась и кинетическая, и потенциальная энергия молекул свинца. Следовательно, механическая энергия, которой обладал шар в начале опыта, не исчезла. Она перешла в энергию молекул.
Кинетическая энергия всех молекул, из которых состоит тело, и потенциальная энергия их взаимодействия составляют внутреннюю энергию тела.
При изучении тепловых явлений учитывают только энергию молекул, потому что главным образом она изменяется в этих явлениях. В дальнейшем, рассматривая внутреннюю энергию тела, мы будем понимать под ней кинетическую энергию теплового движения и потенциальную энергию взаимодействия молекул тела.
Вернёмся к опыту со свинцовым шаром и плитой (см. рис. 2).
При остановке шара механическое движение прекращается, но зато усиливается беспорядочное (тепловое) движение его молекул. Механическая энергия превращается во внутреннюю энергию шара.
Итак, кроме механической энергии, существует ещё один вид энергии. Это внутренняя энергия тела.
Внутренняя энергия зависит от температуры тела, агрегатного состояния вещества и других факторов. (Более подробно это будет изучено в 10 классе.)
Поднимем тело, например мяч, над столом. При этом расстояние между молекулами мяча не меняется. Значит, не меняется и потенциальная энергия взаимодействия молекул. Следовательно, поднимая мяч, мы не изменяем его внутреннюю энергию.
Будем двигать мяч относительно стола. От этого его внутренняя энергия также не изменится.
Следовательно, внутренняя энергия тела не зависит ни от механического движения тела, ни от положения этого тела относительно других тел.
Тело, имея некоторый запас внутренней энергии, одновременно может обладать и механической энергией. Например, пуля, летящая на некоторой высоте над землёй, кроме внутренней энергии, обладает ещё и механической энергией — потенциальной и кинетической.

Летящая пуля кроме внутренней энергии обладает и механической
Кинетическая и потенциальная энергия одной молекулы — очень маленькая величина, ведь масса молекулы мала. Поскольку в теле содержится множество молекул, то внутренняя энергия тела, равная сумме энергий всех молекул, достаточно велика.
Вопросы
1. Какие превращения энергии происходят при подъёме шара и при его падении? 2. Как изменяется состояние свинцового шара и свинцовой плиты в результате их соударения? 3. Какую энергию называют внутренней энергией тела? Зависит ли внутренняя энергия тела от его движения и положения относительно других тел?
УПРАЖНЕНИЕ 1
Какими видами механической энергии обладают молекулы вещества вследствие своего движения?
2. Какое тело обладает большей внутренней энергией: кусок льда при температуре О °С или полученная из этого куска льда вода при О °С?
ЗАДАНИЕ
Положите мячик на край стола. Столкните его. Объясните, почему мячик при отскоке не смог подняться до уровня стола.
Внутренняя энергия тела не является какой-то постоянной величиной. У одного и того же тела она может изменяться.
При повышении температуры внутренняя энергия тела увеличивается, так как увеличивается средняя скорость движения молекул.
Следовательно, возрастает кинетическая энергия молекул этого тела. С понижением температуры, наоборот, внутренняя энергия тела уменьшается.
Таким образом, внутренняя энергия тела меняется при изменении скорости движения молекул.

Попытаемся выяснить, каким способом можно увеличить или уменьшить скорость движения молекул. Для этого проделаем следующий опыт. Укрепим тонкостенную латунную трубку на подставке (рис. 3). Нальём в трубку немного эфира и закроем пробкой. Затем трубку обовьём верёвкой и начнём быстро двигать её то в одну сторону, то в другую. Через некоторое время эфир закипит, и пар вытолкнет пробку. Опыт показывает, что внутренняя энергия эфира увеличилась: ведь он нагрелся и даже закипел.
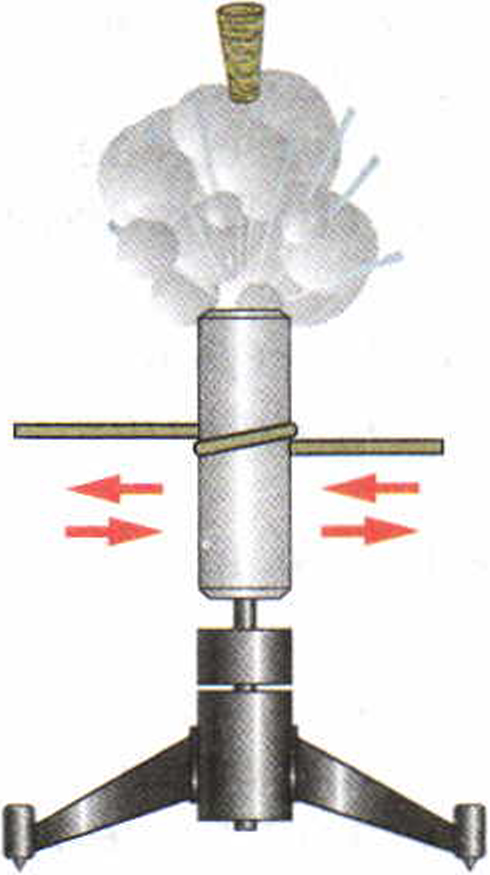
Рис. 3. Увеличение внутренней энергии тела при совершении работы над ним
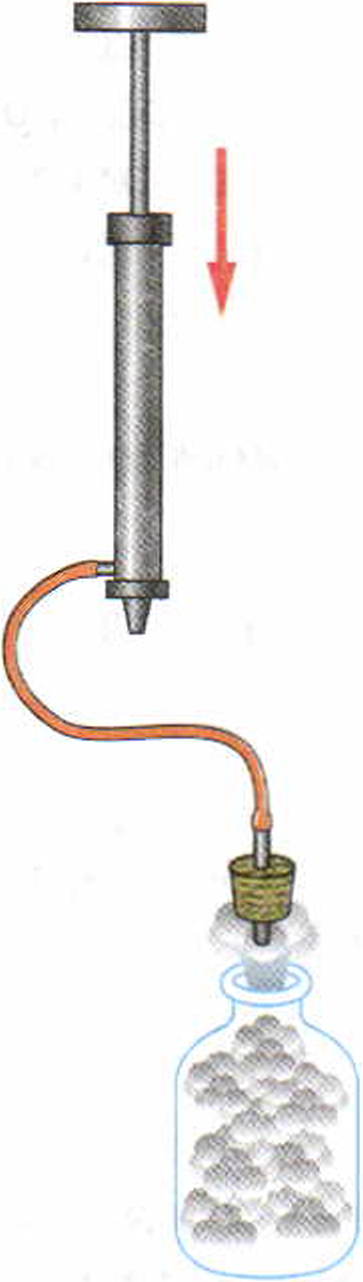
Рис. 4. Уменьшение внутренней энергии тела при совершении работы самим телом
Увеличение внутренней энергии произошло в результате совершения работы при натирании трубки верёвкой.
Нагревание тел происходит также при ударах, разгибании и сгибании, т. е. при деформации. Внутренняя энергия тела во всех приведённых примерах увеличивается.
Следовательно, внутреннюю энергию тела можно увеличить, совершая над телом работу.
Если же работу совершает само тело, то его внутренняя энергия уменьшается.
Проделаем следующий опыт.
В толстостенный стеклянный сосуд, закрытый пробкой, накачаем воздух через специальное отверстие в ней (рис. 4).
Через некоторое время пробка выскочит из сосуда. В момент, когда пробка выскакивает из сосуда, образуется туман. Его появление означает, что воздух в сосуде стал холоднее. Находящийся в сосуде сжатый воздух, выталкивая пробку, совершает работу. Эту работу он совершает за счёт своей внутренней энергии, которая при этом уменьшается. Судить об уменьшении внутренней энергии можно по охлаждению воздуха в сосуде. Итак, внутреннюю энергию тела можно изменить путём совершения работы.
Внутреннюю энергию тела можно изменить и другим способом, без совершения работы. Например, вода в чайнике, поставленном на плиту, закипает. Воздух и различные предметы в комнате нагреваются от радиатора центрального отопления, крыши домов нагреваются лучами солнца и т. п. Во всех этих случаях повышается температура тел, а значит, увеличивается их внутренняя энергия. Но при этом работа не совершается.
Значит, изменение внутренней энергии может происходить не только в результате совершения работы.
Как можно объяснить увеличение внутренней энергии в этих случаях?
Рассмотрим следующий пример.
Опустим в стакан с горячей водой металлическую спицу. Кинетическая энергия молекул горячей воды больше кинетической энергии частиц холодного металла. Молекулы горячей воды при взаимодействии с частицами холодного металла будут передавать им часть своей кинетической энергии. В результате этого энергия молекул воды в среднем будет уменьшаться, а энергия частиц металла будет увеличиваться. Температура воды уменьшится, а температура металлической спицы постепенно увеличится. Через некоторое время их температуры выравняются. Этот опыт демонстрирует изменение внутренней энергии тел.
Итак, внутреннюю энергию тел можно изменить путём теплопередачи.

Изменение внутренней энергии тела путём теплопередачи
Процесс изменения внутренней энергии без совершения работы над телом или самим телом называется теплопередачей.
Теплопередача всегда происходит в определённом направлении: от тел с более высокой температурой к телам с более низкой.
Когда температуры тел выравняются, теплопередача прекращается.
Внутреннюю энергию тела можно изменить двумя способами: совершая механическую работу или теплопередачей.
Теплопередача, в свою очередь, может осуществляться: 1) теплопроводностью; 2) конвекцией:; 3) излучением.
Вопросы
1. Пользуясь рисунком 3, расскажите, как изменяется внутренняя энергия тела, когда над ним совершают работу.
2. Опишите опыт, показывающий, что за счёт внутренней энергии тело может совершить работу.
3. Приведите примеры изменения внутренней энергии тела способом теплопередачи.
4. Объясните на основе молекулярного строения вещества нагревание спицы,
опущенной в горячую воду.
5 Что такое теплопередача?
6. Какими двумя способами можно изменить внутреннюю энергию тела?
УПРАЖНЕНИЕ 2
1. Сила трения совершает над телом работу. Меняется ли при этом внутренняя энергия тела? По каким признакам можно судить об этом?
2. При быстром спуске по канату нагреваются руки. Объясните, почему это происходит.
ЗАДАНИЕ
Положите монету на лист фанеры или деревянную доску. Прижмите монету к доске и двигайте её быстро то в одну, то в другую сторону. Заметьте, сколько раз надо передвинуть монету, чтобы она стала тёплой, горячей. Сделайте вывод о связи между выполненной работой и увеличением внутренней энергии тела.

Передача внутренней энергии от одной части гвоздя к другой при нагревании

В предыдущем параграфе мы выяснили, что при опускании металлической спицы в стакан с горячей водой очень скоро конец спицы становился тоже горячим. Следовательно, внутренняя энергия, как и любой вид энергии, может быть передана от одних тел к другим. Внутренняя энергия может передаваться и от одной части тела к другой. Так, например, если один конец гвоздя нагреть в пламени, то другой его конец, находящийся в руке, постепенно нагреется и будет жечь руку.
Явление передачи внутренней энергии от одной части тела к другой или от одного тела к другому при их непосредственном контакте называется теплопроводностью.

Нагревание стеклянной палочки в горячей воде, свидетельствующее о плохой теплопроводности стекла
Изучим это явление, проделав ряд опытов с твёрдыми телами, жидкостью и газом.
Внесём в огонь конец деревянной палки. Он воспламенится. Другой конец палки, находящийся снаружи, будет холодным. Значит, дерево обладает плохой теплопроводностью.
Поднесём к пламени спиртовки конец тонкой стеклянной палочки. Через некоторое время он нагреется, другой же конец останется холодным. Следовательно, и стекло имеет плохую теплопроводность.
Если же мы будем нагревать в пламени конец металлического стержня, то очень скоро весь стержень сильно нагреется. Удержать его в руках мы уже не сможем.
Значит, металлы хорошо проводят тепло, т. е. имеют большую теплопроводность. Наибольшей теплопроводностью обладают серебро и медь.
Рассмотрим передачу тепла от одной части твёрдого тела к другой на следующем опыте.
Закрепим один конец толстой медной проволоки в штативе. К проволоке прикрепим воском несколько гвоздиков. При нагревании свободного конца проволоки в пламени спиртовки воск будет таять. Гвоздики начнут постепенно отваливаться (рис. 5). Сначала отпадут те, которые расположены ближе к пламени, затем по очереди все остальные.
Выясним, как происходит передача энергии по проволоке. Скорость колебательного движения частиц металла увеличивается в той части проволоки, которая ближе расположена к пламени. Поскольку частицы постоянно взаимодействуют друг с другом, то увеличивается скорость движения соседних частиц. Начинает повышаться температура следующей части проволоки и т. д.
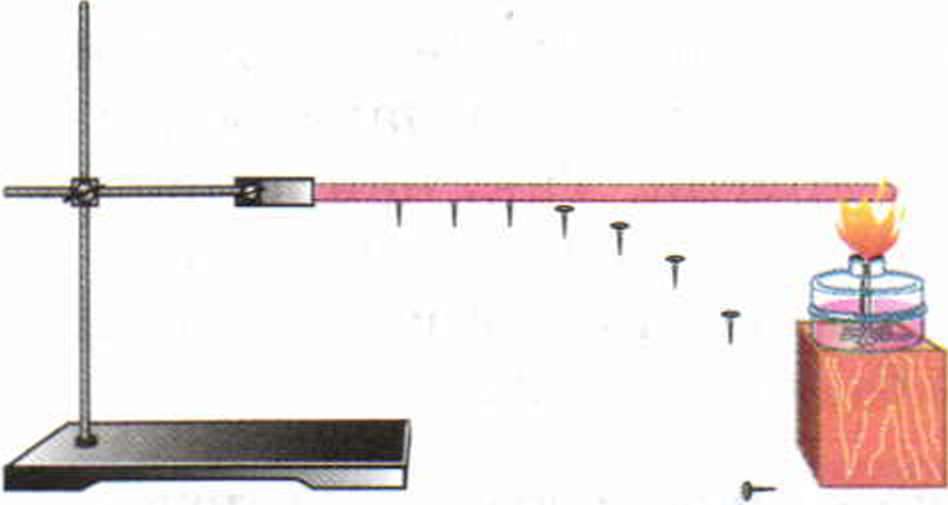
Рис. 5. Передача тепла от одной части твёрдого тела к другой
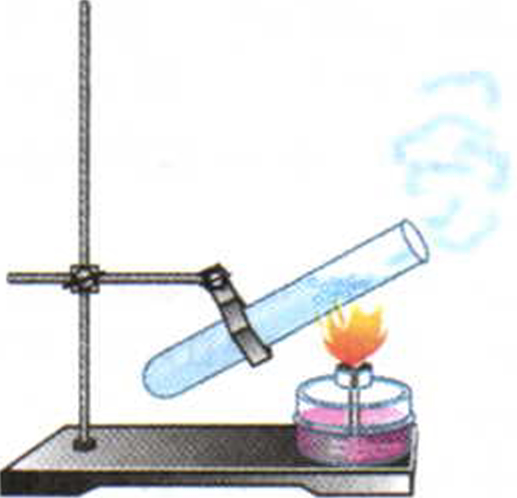
Рис. 6. Теплопроводность жидкости
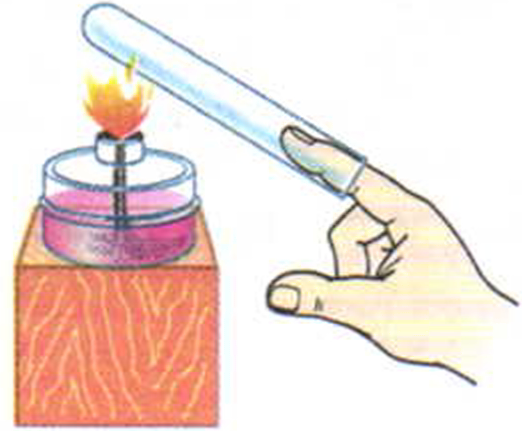
Рис. 7. Теплопроводность газа.
Следует помнить, что при теплопроводности не происходит переноса вещества от одного конца тела к другому.
Рассмотрим теперь теплопроводность жидкостей. Возьмём пробирку с водой и станем нагревать её верхнюю часть. Вода у поверхности скоро закипит, а у дна пробирки за это время она только нагреется (рис. 6). Значит, у жидкостей теплопроводность невелика, за исключением ртути и расплавленных металлов.
Это объясняется тем, что в жидкостях молекулы расположены на больших расстояниях друг от друга, чем в твёрдых телах.
Исследуем теплопроводность газов. Сухую пробирку наденем на палец и нагреем в пламени спиртовки донышком вверх (рис. 7). Палец при этом долго не почувствует тепла.
Это связано с тем, что расстояние между молекулами газа ещё больше, чем у жидкостей и твёрдых тел. Следовательно, теплопроводность у газов ещё меньше.
Итак, теплопроводность у различных веществ различна.
Опыт, изображённый на рисунке 8, показывает, что теплопроводность у различных металлов неодинакова.
Плохой теплопроводностью обладают шерсть, волосы, перья птиц, бумага, пробка и другие пористые тела. Это связано с тем, что между волокнами этих веществ содержится воздух. Самой низкой теплопроводностью обладает вакуум (освобождённое от воздуха пространство). Объясняется это тем, что теплопроводность — это перенос энергии от одной части тела к другой, который происходит при взаимодействии молекул или других частиц. В пространстве, где нет частиц, теплопроводность осуществляться не может.
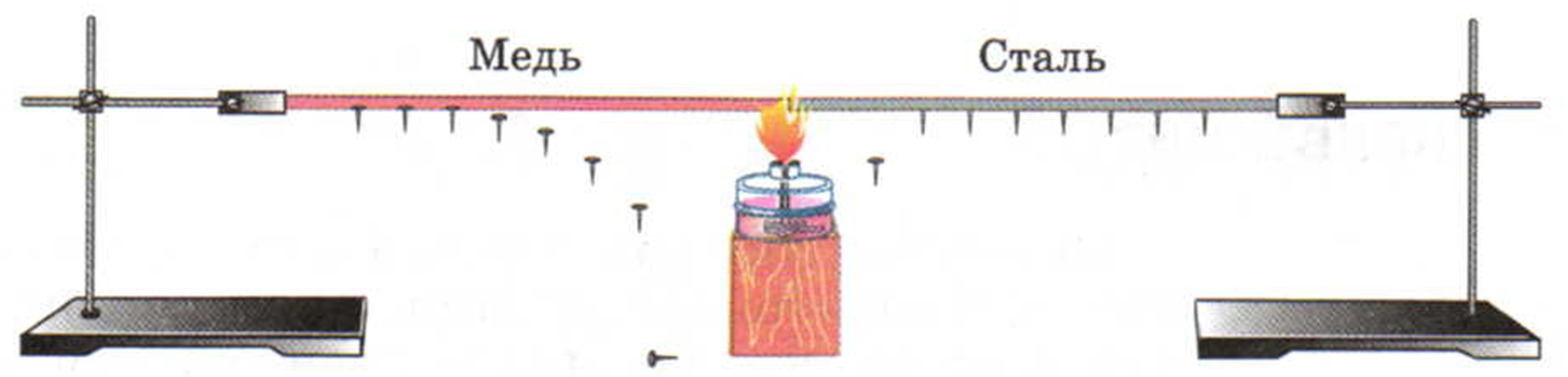
Рис. 8. Теплопроводность разных металлов
Если возникает необходимость предохранить тело от охлаждения или нагревания, то применяют вещества с малой теплопроводностью. Так, для кастрюль, сковородок ручки изготавливают из пластмассы. Дома строят из брёвен или кирпича, обладающих плохой теплопроводностью, а значит, предохраняющих помещения от охлаждения.1. Как происходит передача энергии по металлической проволоке?
2. Объясните опыт (см. рис. 8), показывающий, что теплопроводность меди больше, чем теплопроводность стали.
3 Какие вещества имеют наибольшую и наименьшую теплопроводность? Где их применяют?
4. Почему мех, пух, перья на теле животных и птиц, а также одежда человека защищают от холода?
1. Почему глубокий рыхлый снег предохраняет озимые хлеба от вымерзания?
2. Подсчитано, что теплопроводность сосновых досок в 3,7 раза больше, чем сосновых опилок. Чем объяснить такую разницу?
3. Почему вода не замерзает под толстым слоем льда?
4. Почему выражение «шуба греет» неверно?
ЗАДАНИЕ
Возьмите чашку с горячей водой и одновременно опустите в воду металлическую и деревянную ложки. Какая из ложек быстрее нагреется? Каким способом осуществляется теплообмен между водой и ложками? Как изменяется внутренняя энергия воды и ложек?

Помещая руку над горячей плитой или над горящей электрической лампочкой, можно почувствовать, что над ними поднимаются тёплые струи воздуха.
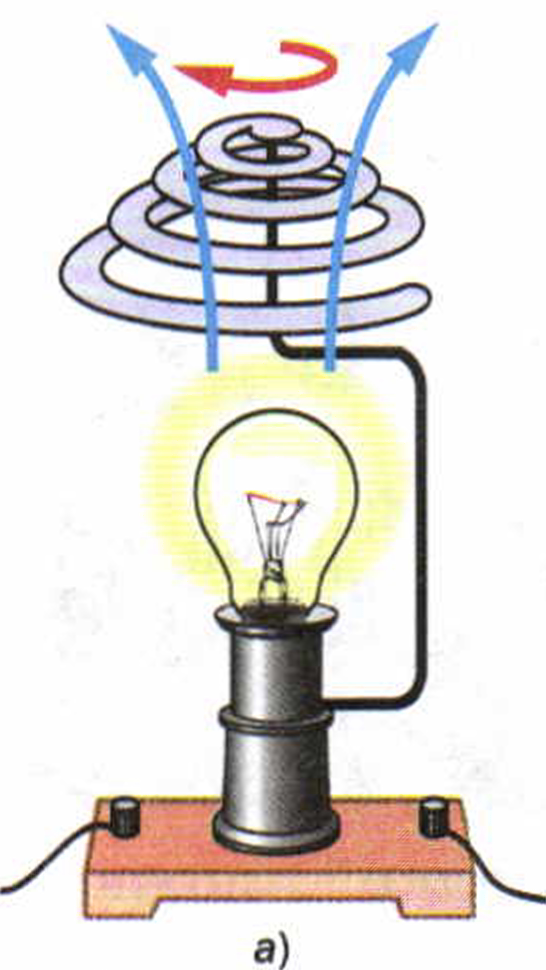
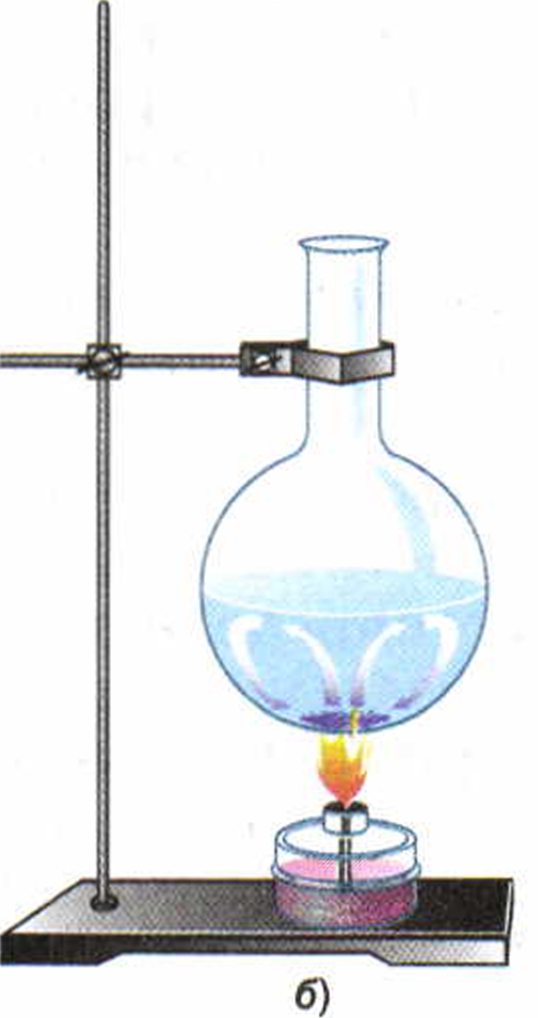
Рис. 9. Конвекция: а — в воздухе; б — в жидкости
Небольшая бумажная вертушка, поставленная над пламенем свечи или электрической лампочкой, под действием поднимающегося нагретого воздуха начинает вращаться (рис. 9, а).
Это явление можно объяснить таким образом. Воздух, соприкасаясь с тёплой лампой, нагревается, расширяется и становится менее плотным, чем окружающий его холодный воздух. Сила Архимеда, действующая на тёплый воздух со стороны холодного снизу вверх, больше, чем сила тяжести, которая действует на тёплый воздух. В результате нагретый воздух «всплывает», поднимается вверх, а его место занимает холодный воздух.
Такие же явления мы наблюдаем и при нагревании жидкости снизу. Нагретые слои жидкости — менее плотные и поэтому более лёгкие — вытесняются вверх более тяжёлыми, холодными слоями. Холодные слои жидкости, опустившись вниз, в свою очередь, нагреваются от источника тепла и вновь вытесняются менее нагретой водой. Благодаря такому движению вся вода равномерно прогревается. Этот процесс становится наглядным, если на дно колбы бросить несколько кристалликов марганцовокислого калия, который окрашивает струи воды в фиолетовый цвет (рис. 9, б).
В описанных опытах мы наблюдали ещё один вид теплопередачи, называемый конвекция (от лат. конвекцио — перенесение).
Следует помнить, что при конвекции энергия переносится самими струями газа или жидкости.
Так, например, в отапливаемой комнате благодаря конвекции поток тёплого воздуха поднимается вверх, а холодного опускается вниз (рис. 10). Поэтому у потолка воздух всегда теплее, чем вблизи пола.
Различают два вида конвекции: естественную (или свободную) и вынужденную. Так, нагревание жидкости, а также воздуха в комнате являются примерами естественной конвекции. Вынужденная конвекция наблюдается, если
перемешивать жидкость мешалкой, ложкой, насосом и т. д.
Если жидкости и газы прогревать не снизу, а сверху (см. рис. 6, 7), то конвекция не происходит. Нагретые слои не могут опуститься ниже холодных, более тяжёлых.
Следовательно, для того чтобы в жидкостях и газах происходила конвекция, необходимо их нагревать снизу.
Конвекция в твёрдых телах происходить не может. Вам уже известно, что частицы в твёрдых телах колеблются около определённой точки, удерживаемые сильным взаимным притяжением. В связи с этим при нагревании твёрдых тел в них не могут образовываться потоки вещества. Энергия в твёрдых телах может передаваться теплопроводностью.
Вопросы
1. Объясните, как и почему происходит перемещение воздуха над нагретой лампой. Объясните, как происходит нагревание воды в колбе, поставленной на огонь. В чём состоит явление конвекции? Чем отличается естественная конвекция от вынужденной? Почему жидкости и газы нагревают снизу? Почему конвекция невозможна в твёрдых телах?

Рис. 10. Нагревание воздуха путём конвекции

1. Почему подвал — самое холодное место в доме?
2. Почему форточки для проветривания комнат помещают в верхней части окна, а радиаторы — у пола?
3. Каким способом охлаждается воздух в комнате зимой при открытой форточке?

Включите настольную лампу и расположите над ней маленькую пушинку. Опишите, что вы наблюдаете. Объясните, с каким видом теплопередачи связано наблюдаемое явление.
Примеры конвекции в природе и технике
Ветры. В атмосфере Земли вследствие неодинакового нагрева воздуха в жарком поясе и в полярных областях возникает мощное конвекционное движение воздуха, образующее постоянно дующие ветры.
Одной из причин образования пассатов — ветров, дующих от субтропических областей к экватору, — является неравномерное нагревание земной поверхности солнцем. Средняя годовая температура на экваторе Земли на 50 °С выше, чем на её полюсах. В экваториальной зоне Земли нагретый воздух поднимается вверх. На его место с севера и юга притекает холодный воздух. Его движение и есть пассат. Потоки холодного воздуха вследствие вращения Земли движутся не вдоль меридиана, а отклоняются. В связи с этим в Северном полушарии пассаты имеют северо-восточное направление, а в Южном — юго-восточное.
Ветры вызывают образование океанических течений. Постоянно дующий в одном направлении ветер приводит в движение верхние слои воды. Они перемещаются в сторону ветра. Тёплые и холодные океанические течения могут служить примерами вынужденной конвекции.
Возникновение ветра на берегах морей — бриза — также объясняется конвекцией. В летние дни суша нагревается солнцем сильнее, чем вода в море. Нагревшийся от суши воздух поднимается вверх. Это происходит потому, что плотность воздуха уменьшается и давление становится меньше давления более холодного воздуха над морем.
На место тёплого воздуха с моря приходит более прохладный. Днём ветер дует поэтому с моря на сушу (дневной бриз). Ночью, наоборот, поверхность суши остывает быстрее, чем вода в море. Ветер меняет своё направление — дует с суши на море (ночной бриз).

Тяга. Вы знаете, что горение топлива без притока свежего воздуха невозможно. Горение топлива прекратится, если в трубу самовара, камина не будет поступать воздух. На практике используют естественный приток воздуха — тягу. На фабриках и заводах, на электростанциях, в котельных установках для усиления тяги устанавливают трубу (рис. 11). Воздух в трубе при горении нагревается, а значит, его плотность уменьшается. Следовательно, давление воздуха, находящегося в топке и трубе, становится меньше давления наружного воздуха. Возникает разность давлений. Вследствие разницы давлений холодный воздух поступает в топку, а тёплый поднимается вверх. Возникает тяга, которая усиливается при увеличении высоты трубы.
Отопление и охлаждение жилых помещений. В современных зданиях устанавливают водяное отопление. По всему зданию проводят систему распределительных труб, а от них вниз идут вертикальные трубы, которые проходят через комнаты здания.
Из этих труб вода поступает в отопительные батареи. Вода отдаёт им своё тепло и возвращается в котёл, где снова нагревается. Так происходит циркуляция воды и прогревание воздуха за счёт конвекции.
Сегодня многие помещения оснащены кондиционерами, которые при необходимости могут не только нагревать помещение, но и охлаждать его.
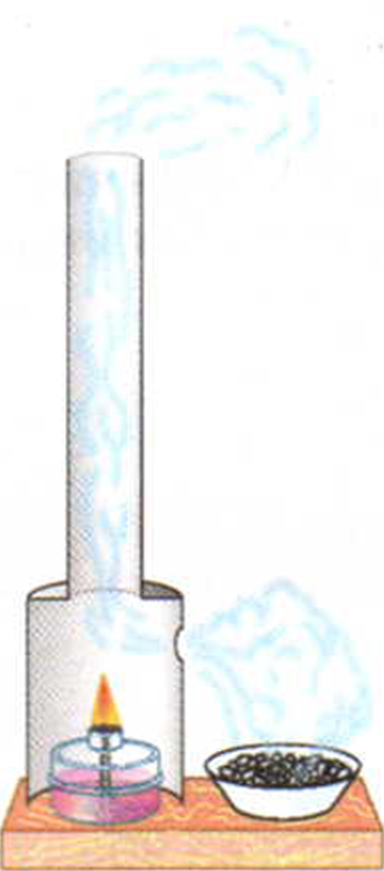
Рис. 11. Модель для демонстрации тяги/


Излучение в природе
Вам хорошо известно, что основным источником тепла на Земле является Солнце. Каким же образом передаётся тепло от Солнца? Ведь Земля находится от него на расстоянии 15 • 107 км. Всё это пространство за пределами нашей атмосферы содержит очень разреженное вещество.
Как известно, в вакууме перенос энергии путём теплопроводности невозможен. Не может происходить он и за счёт конвекции. Следовательно, существует ещё один вид теплопередачи.
Изучим этот вид теплопередачи с помощью опыта.
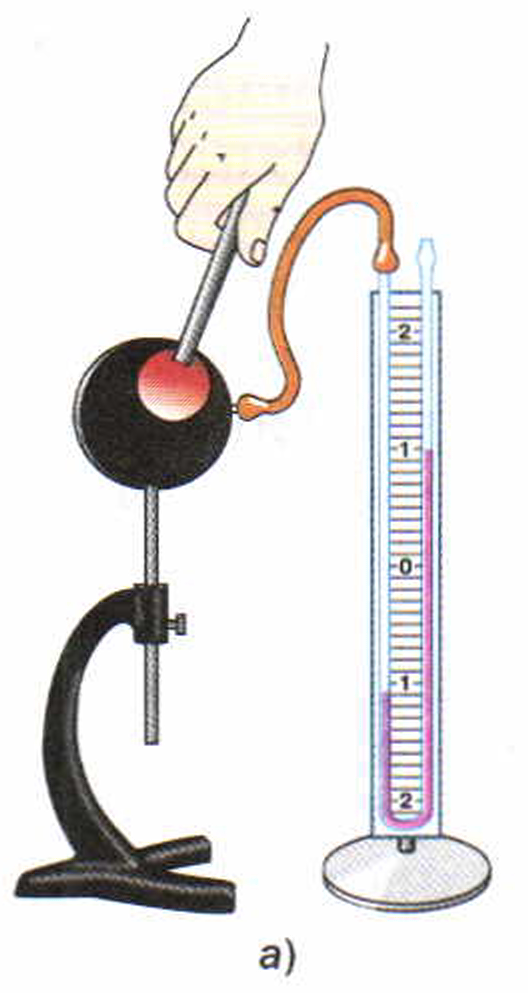
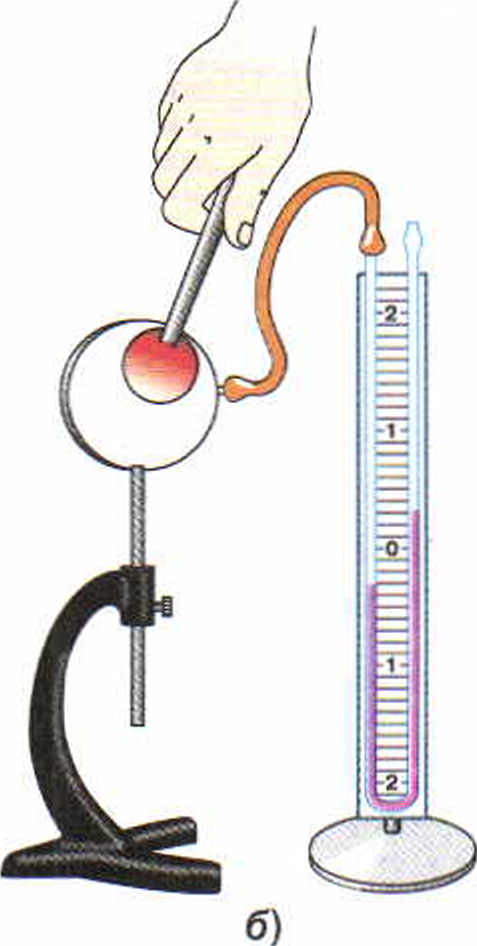
Рис. 12. Передача энергии путём излучения
Соединим жидкостный манометр при помощи резиновой трубки с теплоприёмником (рис. 12).
Если к тёмной поверхности теплоприёмника поднести кусок металла, нагретый до высокой температуры, то уровень жидкости в колене манометра, соединённом с теплоприёмником, понизится (рис. 12, а). Очевидно, воздух в теп-лоприёмнике нагрелся и расширился. Быстрое нагревание воздуха в теплоприёмнике можно объяснить лишь передачей ему энергии от нагретого тела.
Энергия в данном случае передавалась не теплопроводностью. Ведь между нагретым телом и теплоприёмником находился воздух — плохой проводник тепла. Конвекция здесь также не может наблюдаться, поскольку тепло-приёмник находится рядом с нагретым телом, а не над ним. Следовательно, в данном случае передача энергии происходит путём излучения.
Передача энергии излучением отличается от других видов теплопередачи. Она может осуществляться в полном вакууме.
Излучают энергию все тела: и сильно нагретые, и слабо, например, тело человека, печь, электрическая лампочка и др. Но чем выше температура тела, тем больше энергии передаёт оно путём излучения. При этом энергия частично поглощается окружающими телами, а частично отражается. При поглощении энергии тела нагреваются по-разному, в зависимости от состояния поверхности.
Если повернуть теплоприёмник к нагретому металлическому телу сначала тёмной, а затем светлой стороной, то столбик жидкости в колене манометра, соединённом с теплоприёмником, в первом случае (см. рис. 12, а) понизится, а во втором (рис. 12, б) повысится. Это показывает, что тела с тёмной поверхностью лучше поглощают энергию, чем тела, имеющие светлую поверхность.

Серебристая поверхность метеозонда отражает солнечные лучи
В то же время тела с тёмной поверхностью охлаждаются быстрее путём излучения, чем тела со светлой поверхностью. Например, в светлом чайнике горячая вода дольше сохраняет высокую температуру, чем в тёмном.
Способность тел по-разному поглощать энергию излучения используется на практике. Так, поверхность воздушных метеозондов, крылья самолётов красят серебристой краской, чтобы они не нагревались солнцем. Если же, наоборот, необходимо использовать солнечную энергию, например в приборах, установленных на искусственных спутниках Земли, то эти части приборов окрашивают в тёмный цвет.
1. Как на опыте показать передачу энергии излучением? 2. Какие тела лучше, а какие хуже поглощают энергию излучения? 3. Как учитывает человек на практике различную способность тел поглощать энергию излучения?
1. Летом воздух в здании нагревается, получая энергию различными способами: через стены, через открытое окно, в которое входит тёплый воздух, через стекло, которое пропускает солнечную энергию. С каким видом теплопередачи мы имеем дело в каждом случае?
2. Приведите примеры, показывающие, что тела с тёмной поверхностью сильнее нагреваются излучением, чем со светлой.
3. Почему можно утверждать, что от Солнца к Земле энергия не может передаваться конвекцией и теплопроводностью? Каким способом она передаётся?
С помощью уличного термометра измерьте температуру сначала на солнечной стороне дома, затем на теневой. Объясните, почему различаются показания термометра.
Термос. Часто бывает необходимо сохранить пищу горячей или холодной. Чтобы помешать телу охладиться или нагреться, нужно уменьшить теплопередачу. При этом стремятся сделать так, чтобы энергия не




передавалась ни одним видом теплопередачи: теплопроводностью, конвекцией, излучением. В этих целях используют термос (рис. 13).
Он состоит из стеклянного сосуда 4 с двойными стенками. Внутренняя поверхность стенок покрыта блестящим металлическим слоем, а из пространства между стенками сосуда выкачан воздух. Лишённое воздуха пространство между стенками почти не проводит тепло. Металлический же слой, отражая, препятствует передаче энергии излучением. Чтобы защитить стекло от повреждений, термос помещают в специальный металлический или пластмассовый футляр 3. Сосуд закупоривается пробкой 2, а сверху навинчивается колпачок 1.
Теплопередача и растительный мир. В природе и жизни человека растительный мир играет исключительно важную роль. Жизнь всего живого на Земле невозможна без воды и воздуха.
В слоях воздуха, прилегающих к Земле, и почве постоянно происходит изменение температуры. Почва нагревается днём, так как поглощает энергию. Ночью, наоборот, она охлаждается — отдаёт энергию. На теплообмен между почвой и воздухом влияет наличие растительности, а также погода.
Почва, покрытая растительностью, плохо прогревается излучением. Сильное охлаждение почвы наблюдается также в ясные, безоблачные ночи. Излучение от почвы свободно уходит в пространство. Ранней весной в такие ночи наблюдаются заморозки. Во время облачности уменьшается потеря энергии почвы путём излучения. Облака служат экраном.
Для повышения температуры почвы и предохранения посадок от заморозков используют теплицы. Стеклянные рамы или изготовленные из плёнки хорошо пропускают солнечное излучение {видимое). Днём почва нагревается. Ночью невидимое излучение почвы стекло или плёнка пропускают хуже. Почва не замерзает. Теплицы препятствуют также движению тёплого воздуха вверх — конвекции.
Вследствие этого температура в теплицах выше, чем в окружающем пространстве.
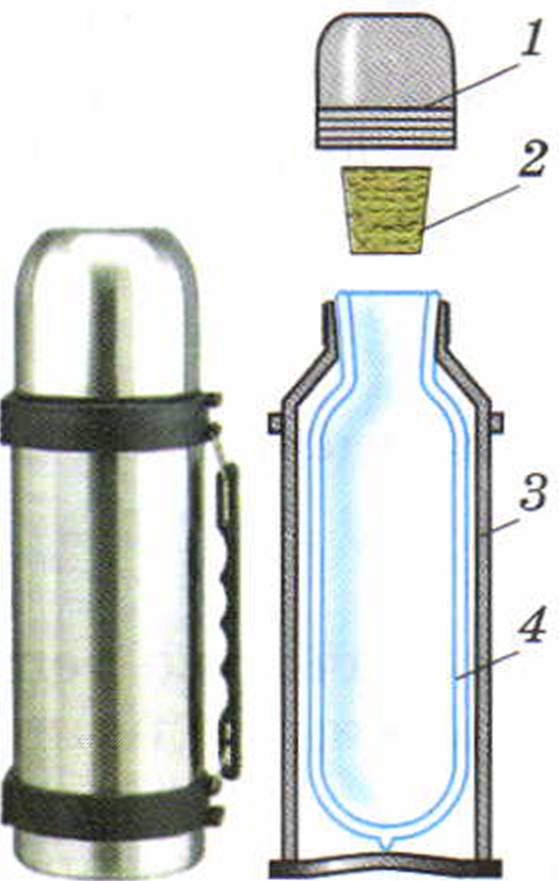
Рис. 13. Устройство термоса

Вам уже известно, что внутренняя энергия тела может изменяться как путём совершения работы, так и путём теплопередачи (без совершения работы). Если изменение внутренней энергии происходит путём теплопередачи, то переход энергии от одних тел к другим осуществляется теплопроводностью, конвекцией или излучением.
Энергия, которую получает или теряет тело при теплопередаче, называется количеством теплоты.
Для того чтобы вычислить количество теплоты, необходимо узнать, от каких величин оно зависит.
Будем нагревать от двух одинаковых горелок два сосуда (рис. 14). В одном сосуде находится 1 кг воды, а в другом — 2 кг. Начальная температура воды в обоих сосудах одинакова. Мы заметим, что за одно и то же время во втором сосуде вода нагреется на меньшее число градусов, хотя оба сосуда получают одинаковое количество теплоты.
Следовательно, количество теплоты, которое необходимо для нагревания тела, зависит от его массы.
Итак, чем больше масса тела, тем большее количество теплоты надо затратить, чтобы изменить его темпера-туру на одно и то же число градусов.
При остывании тело передаёт окружающим предметам тем большее количество теплоты, чем больше его масса.
Вам хорошо известно, что, если необходимо нагреть полный чайник (с водой) до температуры 50 °С, потребуется меньше времени, чем для нагревания чайника с водой той же массы до 100 °С. В первом случае воде будет передано меньшее количество теплоты, чем во втором.
Следовательно, количество теплоты, которое необходимо для нагревания, зависит от того, на сколько градусов нагревается тело. Это значит, что количество теплоты зависит от разности температур тела.
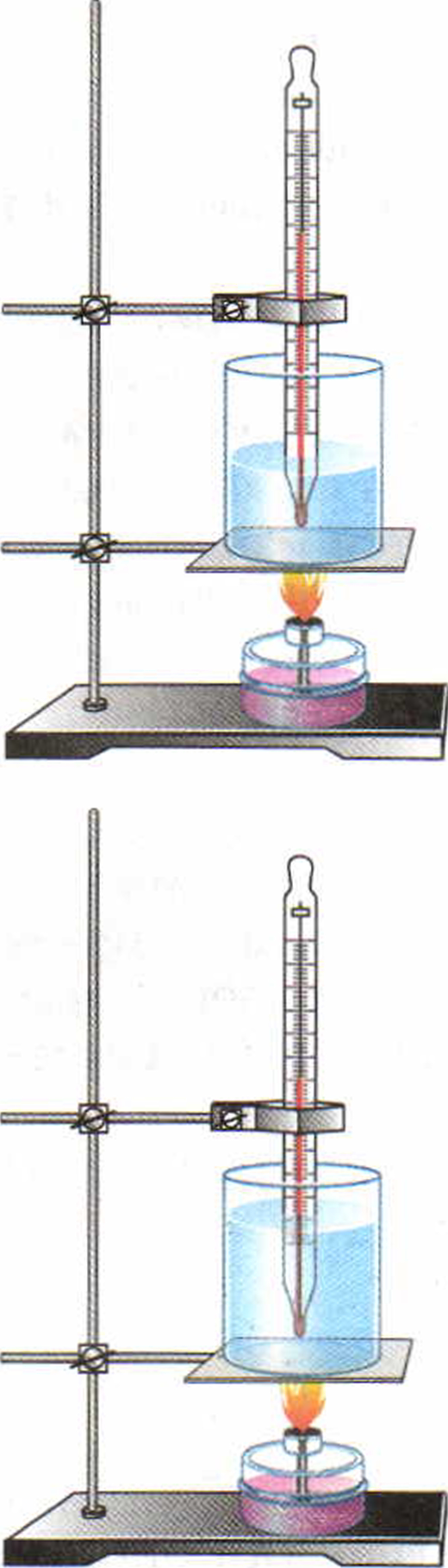
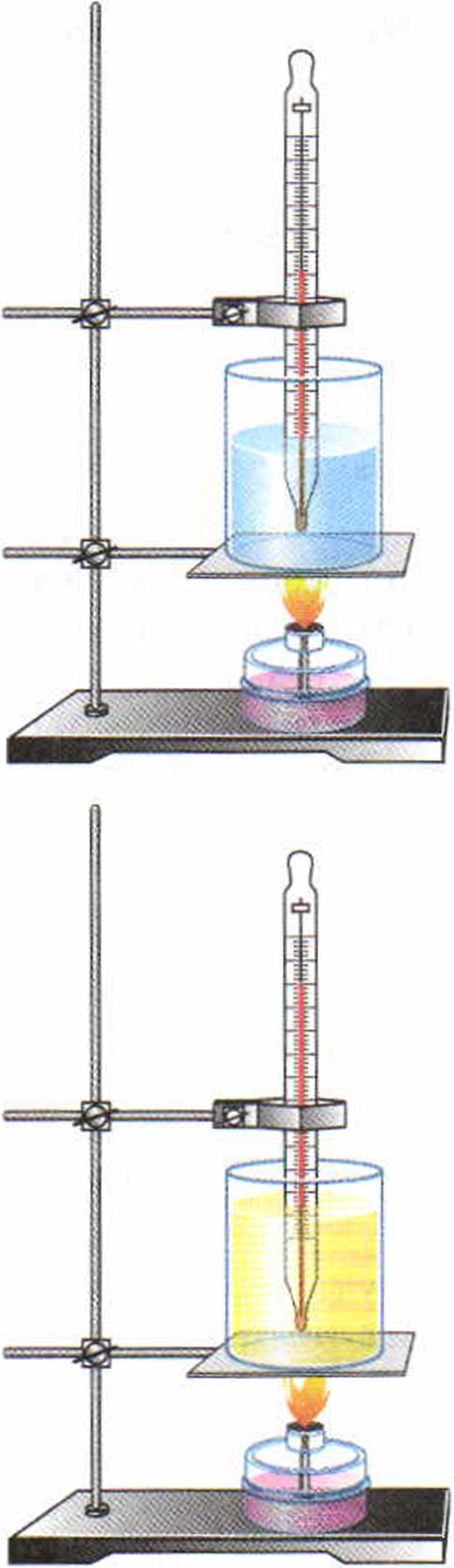
Рис. 14. Нагревание воды разной массы. Рис. 15. Нагревание разных веществ равной массы
Но можно ли рассчитать количество теплоты, необходимое для нагревания не воды, а другого вещества, например свинца, железа, масла и т. д.?Нальём в один сосуд воду, а в другой такой же сосуд — растительное масло (рис. 15). Массы воды и масла возьмём равные. Оба сосуда будем нагревать на одинаковых горелках. Опыт начнём при одинаковой начальной температуре воды и растительного масла. Измерив через некоторое время (например, 5 мин) температуру нагревшихся воды и масла, мы увидим, что масло имеет более высокую температуру» чем вода, хотя обе жидкости получили от горелок равные количества теплоты.
Из опыта нетрудно сделать вывод, что для нагревания равных масс воды и масла на одинаковую температуру требуется различное количество теплоты. Для масла требуется количества теплоты меньше, для воды больше.
Следовательно, количество теплоты, которое необходимо для нагревания тела, зависит от того, из какого вещества оно состоит, т. е. от рода вещества.
Итак, количество теплоты, которое необходимо для нагревания тела (или выделяемое при остывании), зависит от массы этого тела, от изменения его температуры и рода вещества.
Количество теплоты обозначают буквой Q. Как и всякий другой вид энергии, количество теплоты измеряют в джоулях (Дж) или в килоджоулях (кДж).
1 кДж = 1000 Дж.
Однако измерять количество теплоты учёные стали задолго до того, как в физике появилось понятие энергии. Тогда была установлена особая единица для измерения количества теплоты — калория (кал) или килокалория
(ккал). (Калория — от лат. калор — тепло, жар.)
1 ккал = 1000 кал.
Калория — это количество теплоты, которое необходимо для нагревания 1 г воды на 1°С.
1 кал = 4,19 Дж » 4,2 Дж.
1 ккал = 4190 Дж ~ 4200 Дж » 4,2 кДж.
Что такое количество теплоты? 2 Как зависит количество теплоты от изменения температуры тела? 3. Почему нельзя только по изменению температуры тела судить о полученном им количестве теплоты?
Как зависит количество теплоты от массы тела? 5, Опишите опыт, показывающий, что количество теплоты зависит от рода вещества, из которого состоит тело. б. Какими единицами измеряют внутреннюю энергию и количество теплоты?
Утюг нагрет до 80 °С, а батарея отопления — до 40 °С. Можно ли утверждать, что утюг, остывая до комнатной температуры, передаст окружающей среде большее количество теплоты?
2. Какое тело отдаст большее количество теплоты: ртуть в термометре или ртуть в бутыли объёмом 0,5 л при понижении их температуры на 2 °С?
Мы узнали, от каких величин зависит количество теплоты и каковы единицы его измерения. Нам известно, что для нагревания тел одинаковой массы, взятых при одинаковой температуре, на одну и ту же величину требуется разное количество теплоты. Так, для нагревания 1 кг воды на 1 °С требуется количество теплоты, равное 4200 Дж. Если нагревать 1 кг серебра на 1 °С, то потребуется 250 Дж.




Физическая величина, численно равная количеству теплоты, которое необходимо передать телу массой 1 кг для того, чтобы его температура изменилась на 1 °С, называется удельной теплоёмкостью вещества.
Удельная теплоёмкость обозначается буквой с и измеряется в Д* .
КГ • L кг • °С
Так, например, удельная теплоёмкость цинка равна 400.
Это означает, что для нагревания цинка массой 1 кг на 1 °С необходимо количество теплоты, равное 400 Дж. При охлаждении цинка массой 1 кг на 1 °С выделится количество теплоты, равное 400 Дж. Это означает, что если меняется температура цинка массой 1 кг на 1 °С, то он или поглощает, или выделяет количество теплоты, равное 400 Дж.
|
Вещество |
„ Дж ’ кг•°С |
Вещество |
„ Дж ’ кг•°С |
Вещество |
„ Дж ’ кг-°С |
|
Золото |
130 |
Железо |
460 |
Масло под | |
|
Ртуть |
140 |
Сталь |
500 |
солнечное |
1700 |
|
Свинец |
140 |
Чугун |
540 |
Лёд |
2100 |
|
Олово |
230 |
Графит |
750 |
Керосин |
2100 |
|
Серебро Медь |
250 400 |
Стекло лабораторное |
840 |
Эфир Дерево (дуб) |
2350 2400 |
|
Цинк |
400 |
Кирпич |
880 |
Спирт |
2500 |
|
Латунь |
400 |
Алюминий |
920 |
Вода |
4200 |
Следует помнить, что удельная теплоёмкость вещества, находящегося в различных агрегатных состояниях, различна.
Например, ртуть в жидком состоянии имеет
удельную теплоёмкость, равную 138 ■, а в
КГ * с
твёрдом состоянии — 129 —к— (при -120 °С).
КГ * с
Удельная теплоёмкость воды самая большая — 4200 —. В связи с этим вода в морях кг • С
и океанах, нагреваясь летом, поглощает большое количество теплоты. Поэтому в районах,
Таблица 1. Удельная теплоёмкость некоторых веществ
расположенных вблизи водоёмов, летом не бывает очень жарко, а зимой очень холодно. Это связано с тем, что зимой вода остывает и отдаёт большое количество теплоты. Из-за высокой удельной теплоёмкости воду широко используют в технике и быту. Например, в отопительных системах домов, при охлаждении деталей во время их обработки на станках, в медицине (в грелках)и др.
1. Удельная теплоёмкость свинца равна 140 кг^тс . Что это означает?
2. Для нагревания 1 кг золота на 1СС требуется 130 Дж. Какова удельная теплоёмкость золота?
В таблице 1 найдите жидкости. Какая из жидкостей при одинаковых условиях будет нагреваться быстрее?
На практике часто пользуются тепловыми расчётами. Например, при строительстве зданий необходимо учитывать, какое количество теплоты должна отдавать зданию вся система отопления. Следует также знать, какое количество теплоты будет уходить в окружающее пространство через окна, стены, двери.
Покажем на примерах, как нужно вести простейшие расчёты.
Итак, необходимо узнать, какое количество теплоты получила при нагревании медная де-




1. Что называется удельной теплоёмкостью вещества? 2. Что является единицей удельной теплоёмкости вещества? 3. Почему близость водоёмов влияет на температуру воздуха? 4. Почему чаще всего вода используется в системе отопления, для охлаждения двигателей?
таль. Её масса 2 кг, а температура увеличивалась от 20 до 280 °С. Вначале по таблице 1 определим удельную теплоёмкость меди ^см =
= 400)• Это означает, что на нагревание
детали из меди массой 1 кг на 1 °С потребуется 400 Дж. Для нагревания медной детали массой 2 кг на 1 °С необходимо в 2 раза большее количество теплоты — 800 Дж. Температуру медной детали необходимо увеличить не на 1 °С, а на 260 °С, значит, потребуется в 260 раз большее количество теплоты, т. е. 800 Дж* 260 = = 208 000 Дж.
Чтобы рассчитать количество теплоты, необходимое для нагревания тела или выделяемое им при охлаждении, следует удельную теплоёмкость умножить на массу тела и на разность между конечной и начальной температурами.
Если обозначить массу т, разность между конечной (t2) и начальной (£х) температурами — t2 - tl7 получим формулу для расчёта количества теплоты:
Q = cm(t2 - *j).
Пример 1. В железный котёл массой 5 кг налита вода массой 10 кг. Какое количество теплоты нужно передать котлу с водой для изменения их температуры от 10 до 100 °С?
При решении задачи нужно учесть, что оба тела — и котёл, и вода — будут нагреваться вместе. Между ними происходит теплообмен. Их температуры можно считать одинаковыми, т. е. температура котла и воды изменяется на 100 °С - 10 °С = 90 °С. Но количества теплоты, полученные котлом и водой, не будут одинаковыми. Ведь их массы и удельные теплоёмкости различны.
Запишем условие задачи и решим её.
Q = cm(t2 - ij)
Нагревание воды в котелке

Q2 = 4200
Дж кг - °(
Решение:
Количество теплоты, полученное котлом, равно:
Q1 = c1m1(t2-t1),
Q = 460 • 5 кг • 90 °С «
кг • °С
« 207 000 Дж = 207 кДж. Количество теплоты, полученное водой, равно:
Q2 = С2Ш2{t2 ~ ^i)>
• 10 кг • 90 °С * з 780 000 Дж =
= 3780 кДж.
На нагревание и котла, и воды израсходовано количество теплоты: Q = Qx + Q2,
Q = 207 кДж + 3780 кДж = 3987 кДж.
Ответ: Q = 3987 кДж.
Пример 2. Смешали воду массой 0,8 кг, имеющую температуру 25 °С, и воду при температуре 100 °С массой 0,2 кг. Температуру полученной смеси измерили, и она оказалась равной 40 °С. Вычислите, какое количество теплоты отдала горячая вода при остывании и получила холодная вода при нагревании. Сравните эти количества теплоты.
Запишем условие задачи и решим её.
Решение:
Горячая вода остыла от 100 до 40 °С, при этом она отдала количество теплоты:
Q i = c1m1(t2-t),
Q =4200 -0,2 кгх
А кг • С
х (100 °С - 40 °С) =
= 50 400 Дж.
Холодная вода нагрелась с 25 до 40 °С и полу-
Дано:
ml = 0,2 кг т2 = 0,8 кг
с, = с, = 4200 1 2 кг • °С
t1 = 25 °С ^2 = 100 °С * = 40 °С
Q1-? Q2-?
чила количество теплоты:
^2 = ^l)»
Дано:
/711 = 5 КГ
С = 460 -Щ-
1 кг•°С
т.2 = 10 кг
Со = 4200 -5^
2 кг•°С
^ = 10 °с t2 = 100 °с
Q-?

Q2 = 4200 ЛЦр -0,8 кг-(40 °С - 25 °С) =
кг • v
= 50 400 Дж.
Ответ: = 50 400 Дж, Q2 = 50 400 Дж.
Мы видим, что количество теплоты, отданное горячей водой, и количество теплоты, полученное холодной водой,равны между собой. Это не случайный результат. Опыт показывает, что если между телами происходит теплообмен, то внутренняя энергия всех нагревающихся тел увеличивается на столько, на сколько уменьшается внутренняя энергия остывающих тел.
При проведении опытов обычно получается, что отданная горячей водой энергия больше энергии, полученной холодной водой. Это объясняется тем, что часть энергии передаётся окружающему воздуху, а часть энергии — сосуду, в котором смешивали воду. Равенство отданной и полученной энергий будет тем точнее, чем меньше потерь энергии допускается в опыте. Если подсчитать и учесть эти потери, то равенство будет точным.
1. Что нужно знать, чтобы вычислить количество теплоты, полученное телом при нагревании? 2 Объясните на примере, как рассчитывают количество теплоты, сообщённое телу при его нагревании или выделяющееся при его охлаждении. 3. Напишите формулу для расчёта количества теплоты. 4. Какой вывод можно сделать из опыта по смешиванию холодной и горячей воды? Почему на практике эти энергии не равны?
Какое количество теплоты требуется для нагревания воды массой 0,1 кг на 1 °С?
2. Рассчитайте количество теплоты, необходимое для нагревания: а) чугунного утюга массой 1,5 кг для изменения его температуры на 200 °С; б) алюминиевой ложки массой 50 г от 20 до 90 °С; в) кирпичного камина массой 2 т от 10 до 40 °С.
3. Какое количество теплоты выделилось при остывании воды, объём которой 20 л, если температура изменилась от 100 до 50 °С?


Известно, что источником энергии, которая используется в промышленности, на транспорте, в сельском хозяйстве, в быту, является топливо. Это уголь, нефть, торф, дрова, природный газ и др. При сгорании топлива выделяется энергия. Попытаемся выяснить, за счёт чего выделяется при этом энергия.
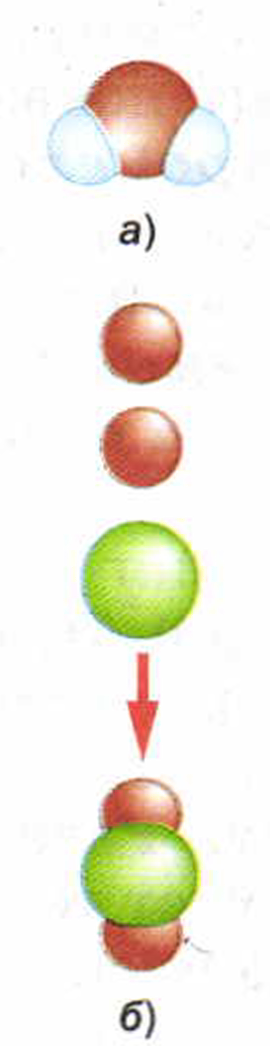
Вспомним строение молекулы воды (рис. 16, а). Она состоит из одного атома кислорода и двух атомов водорода. Если молекулу воды разделить на атомы, то при этом необходимо преодолеть силы притяжения между атомами, т. е. совершить работу, а значит, затратить энергию. И наоборот, если атомы соединяются в молекулу, энергия выделяется.
Использование топлива основано как раз на явлении выделения энергии при соединении атомов. Так, например, атомы углерода, содержащиеся в топливе, при горении соединяются с двумя атомами кислорода (рис. 16, б). При этом образуется молекула оксида углерода — углекислого газа — и выделяется энергия.
При расчёте двигателей инженеру необходимо точно знать, какое количество теплоты может выделить сжигаемое топливо. Для этого надо опытным путём определить, какое количество теплоты выделится при полном сгорании одной и той же массы топлива разных видов.
Удельная теплота сгорания обозначается буквой q. Единицей удельной теплоты сгорания является 1 — .
кг
Удельную теплоту сгорания определяют на опыте с помощью довольно сложных приборов.
Рис. 16. Строение молекул: а — воды; б — соединение атома углерода и двух атомов кислорода в молекулу углекислого газа

Физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой 1 кг, называется удельной теплотой сгорания топлива.
Результаты опытных данных приведены в таблице 2.
|
Вещество |
9,32! ’ КГ |
Вещество |
9.32! КГ |
|
Порох |
0,38 *107 |
Древесный уголь |
3,4-107 |
|
Дрова сухие |
1,0-107 |
Природный газ |
4,4-107 |
|
Торф |
1,4-107 |
Нефть |
4,4-107 |
|
Каменный уголь |
2,7-107 |
Бензин |
4,6-107 |
|
Спирт |
2,7- 107 |
Керосин |
4,6-107 |
|
Антрацит |
3,0-107 |
Водород |
12•107 |
Из этой таблицы видно, что удельная теплота сгорания, например, бензина 4,6 • 107 . Это значит, что при полном сгорании бензина массой 1 кг выделяется 4,6 • 107 Дж энергии.
Общее количество теплоты Q, выделяемое при сгорании т кг топлива, вычисляется по формуле
Q = qm.

1. Какое количество теплоты выделяется при полном сгорании древесного угля массой 15 кг; спирта массой 200 г?
2. Сколько теплоты выделится при полном сгорании нефти, масса которой 2,5 т; керосина, объём которого равен 2 л, а плотность 800 ^ ?
3. При полном сгорании сухих дров выделилось 50 000 кДж энергии. Какая масса дров сгорела?
Таблица 2. Удельная теплота сгорания некоторых видов топлива
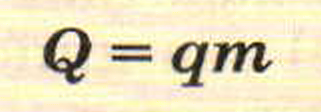

1. Что такое удельная теплота сгорания топлива? 2. В каких единицах измеряют удельную теплоту сгорания топлива? 3. Что означает выражение «удельная теплота сгорания топлива равна 1,4*10'^»?
4. Как вычисляют количество теплоты, выделяемое при сгорании топлива?

■ Используя таблицу 2, постройте столбчатую диаграмму для удельной теплоты сгорания дров, спирта, нефти, водорода, выбрав масштаб следующим образом: ширина прямоугольника — 1 клетка, высота 2 мм соответствует 10 Дж.

Превращение кинетической энергии мяча в потенциальную
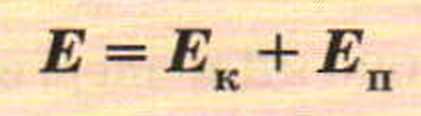

Явления превращения энергии в механических процессах были рассмотрены в § 2. Напомним некоторые из них.
Подбрасывая вверх камень или мяч, мы сообщаем им энергию движения — кинетическую энергию.
Поднявшись до некоторой высоты, предмет останавливается, а затем начинает падать. В момент остановки (в верхней точке) вся кинетическая энергия полностью превращается в потенциальную. При движении тела вниз происходит обратный процесс. Потенциальная энергия превращается в кинетическую.
При этих превращениях полная механическая энергия, т. е. сумма потенциальной и кинетической энергии, остаётся неизменной. Если принять, что потенциальная энергия у поверхности Земли равна нулю, то сумма кинетической и потенциальной энергии тела на любой высоте во время подъёма или падения будет равна
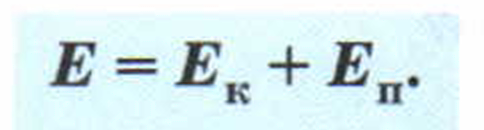
Полная механическая энергия, т. е. сумма потенциальной и кинетической энергии тела, остаётся постоянной, если действуют только силы упругости и тяготения и отсутствуют силы трения.

В этом и заключается закон сохранения механической энергии.

Использование энергии Солнца: а — нагревание поверхности Земли; б — поглощение солнечной энергии растениями и превращение её в химическую энергию

Освещение улиц лампами на солнечных батареях

а)
б)

Во всех явлениях, происходящих в природе, энергия не возникает и не исчезает. Она только превращается из одного вида в другой, при этом её значение сохраняется.
Когда мы изучали падение свинцового шара на свинцовую доску, то наблюдали превращение механической энергии во внутреннюю.
Следовательно, механическая и внутренняя энергия могут переходить от одного тела к другому.
Этот вывод справедлив для всех тепловых процессов. При теплопередаче, например, тело более нагретое отдает энергию, а тело менее нагретое получает энергию.
При сгорании топлива в двигателе машины внутренняя энергия топлива превращается в механическую энергию движения.
При переходе энергии от одного тела к другому или при превращении одного вида энергии в другой энергия сохраняется.
Примером, подтверждающим сделанный вывод, служит опыт по смешиванию холодной и горячей воды (см. лаб. работу № 1) при условии, что мы не допустим перехода теплоты к другим телам. В опыте количество теплоты, отданное горячей водой, равнялось количеству теплоты, полученному холодной водой.
Изучение явлений превращения одного вида энергии в другой привело к открытию одного из основных законов природы — закона сохранения и превращения энергии.
Исследуя явления природы, учёные всегда руководствуются этим законом.
Теперь мы можем сказать, что энергия не может появиться у тела, если оно не получило её от другого тела. Для иллюстрации этого закона природы рассмотрим несколько примеров.
Солнечные лучи несут определённый запас энергии. Падая на поверхность Земли, лучи нагревают её. Энергия солнечных лучей при этом превращается во внутреннюю энергию почвы и тел, находящихся на поверхности Зем-

Газонный фонарь на солнечных батарейках
ли. Воздушные массы, нагревшись от поверхности Земли, приходят в движение — появляется ветер. Происходит превращение внутренней энергии, которой обладают воздушные массы, в механическую энергию.
Часть энергии солнечных лучей поглощается на поверхности земли листьями растений. При этом в растениях происходят сложные химические реакции. В результате образуются органические соединения, т. е. происходит превращение энергии, переносимой солнечными лучами, в химическую энергию.
Превращение внутриатомной энергии в другие виды энергии находит применение на практике. Атомную энергию, например, преобразуют в электрическую на атомных электростанциях (АЭС).
Закон сохранения энергии представляет научную основу для разнообразных расчётов во всех областях науки и техники. Следует учитывать, что полностью внутреннюю энергию нельзя превратить в механическую.

Молот копра при падении ударяет о сваю и забивает её в землю. Какие превращения и переходы энергии при этом происходят? (Следует учесть, что свая и почва нагреваются при ударе.)
2. Какие превращения кинетической энергии автомобиля происходят при торможении?
Два одинаковых стальных шарика падают с одинаковой высоты. Один падает на стальную плиту и отскакивает вверх, другой попадает в песок и застревает в нём. Какие переходы энергии происходят в каждом случае?
Опишите все превращения и переходы энергии, которые происходят при натирании трубки с эфиром, закрытой пробкой (см. рис. 3).
1. Приведите примеры превращения механической энергии во внутреннюю и внутренней в механическую.
2. Приведите примеры перехода энергии от одного тела к другому.
3. Какой опыт показывает, что при переходе внутренней энергии от одного тела к другому её значение сохраняется?
4. В чём состоит закон сохранения энергии?
5. Какое значение имеет закон сохранения энергии в науке и технике?


Использование энергии Солнца на Земле
Источником большей части энергии, которой пользуется человек, является Солнце. За счёт солнечной энергии поддерживается средняя годовая температура на Земле около 15 °С. Поток тепла и света, идущий от Солнца, обусловливает саму возможность жизни на нашей планете. Мощность солнечного излучения, падающего на всю земную поверхность, так велика, что для её замены понадобилось бы около 30 миллионов мощных электростанций.
Стоит только представить себе, что произошло бы на Земле, если бы солнце каждый день не освещало Землю! Мы знаем такие места на Земле, которые слабо нагреваются солнцем. Это Арктика и Антарктика. Там лютый холод, вечный лёд и снег.
Великий непрерывный круговорот воды на Земле совершается за счёт энергии Солнца: вода морей, озёр и рек испаряется, пар, поднявшись вверх, сгущается в облака, переносится ветром в разные места Земли и выпадает в виде осадков. Эти осадки питают реки, которые снова несут свои воды в моря и океаны.
Вследствие неравномерного нагрева поверхности Земли Солнцем возникают ветры. Под действием ветров и приносимой ими влаги постепенно разрушаются огромные горные массивы. Энергия рек используется человеком для получения электроэнергии, передвижения судов, энергия ветра — в ветряных двигателях.
Всё, что происходит на Солнце, самым непосредственным образом сказывается на Земле. Вся жизнь на Земле — жизнь растений и животных — зависит от Солнца. В растениях происходит превращение солнечной энергии в химическую энергию. Чтобы понять это, обратимся к опыту.
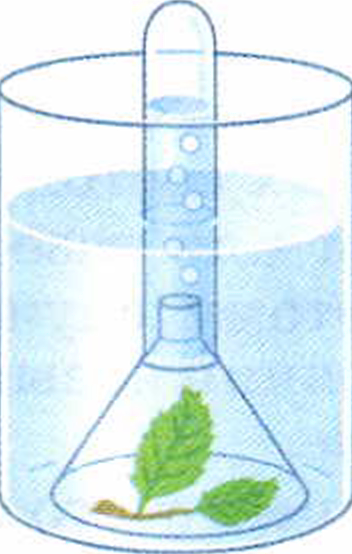
Перевёрнутая воронка помещена в стакан с водой.
химическую энергию и органическое вещество. Кислород выделяется в
В воронке находится лист растения, окружённый воздухом. Если растение освещать солнцем, то можно обнаружить, что из воронки будет выходить кислород (рис. 17). Как объяснить наблюдаемое явление?
В зелёный лист растения проникают молекулы оксида углерода (IV), которые всегда находятся в воздухе. В результате химической реакции, в которой участвуют оксид углерода (IV) и вода, содержащаяся в листе, образуются молекулы кислорода
Рис. 17. Превращение солнечной энергии в
окружающий воздух, а органическое вещество, содержащее углерод, остаётся в листе растения.
Но мы знаем, что для разложения молекулы на атомы нужно затратить энергию (§ 10). Откуда берётся эта энергия? Если описанный выше опыт производить, не освещая лист растения солнцем, то химической реакции не произойдёт. Значит, разложение оксида углерода (IV) в зелёном листе растения происходит благодаря солнечной энергии.
Каменный уголь представляет собой окаменевшие в земле остатки лесов, когда-то буйно росших на больших пространствах Земли. Значит, и в нём запасена энергия Солнца. В болотах из отмирающих растений образуются пласты торфа, используемого как топливо.
Энергия животных, питающихся растениями, и энергия человека — всё это преобразованная солнечная энергия.
Всё шире используется преобразование энергии солнечного излучения в электроэнергию. На поверхности космических кораблей устанавливают солнечные батареи, которые улавливают солнечную энергию и при помощи фотоэлектрических преобразователей превращают её в электроэнергию, которая поступает в единую систему электропитания корабля. Общая полезная площадь солнечной батареи достигает нескольких десятков квадратных метров.
В областях нашей страны, где велико число ясных солнечных дней в году, солнечное излучение используют для нагревания воды, получения водяного пара.
Человечество научилось использовать дополнительный источник энергии на Земле — атомную энергию, непосредственно не связанную с Солнцем.
В зависимости от условий одно и то же вещество может находиться в различных состояниях, например в твёрдом, жидком или газообразном. Наглядным примером этому служат лёд, вода и водяной пар. Эти состояния называют агрегатными состояниями.
Переход вещества из одного агрегатного состояния в другое широко используют в практике. В металлургии, например, плавят металлы, чтобы получить из них сплавы: чугун, сталь, бронзу, латунь и др. Пар, полученный из воды при её нагревании, используют на электростанциях в паровых турбинах и для многих других технических целей. Сжиженными газами пользуются в холодильных установках.




Агрегатные состояния ртути: а — твёрдое (сульфид ртути); б — жидкое; в — газообразное
В природе изменение агрегатных состояний происходит в широких масштабах. С поверхности океанов, морей, озёр и рек испаряется вода, а при охлаждении водяного пара образуются облака, роса, туман или снег. Реки и озёра зимой замерзают, а весной снег и лёд тают.
Для понимания процессов, происходящих в природе, и умения управлять многими из них необходимо знать, когда, при каких условиях вещество находится в том или ином агрегатном состоянии. Следует изучить свойства каждого из этих состояний, а также знать, при каких условиях происходит переход вещества из одного агрегатного состояния в другое.
Мы уже знаем, что молекулы одного и того же вещества в твёрдом, жидком и газообразном состоянии ничем не отличаются друг от друга. То или иное агрегатное состояние вещества определяется расположением, характером движения и взаимодействия молекул.
В газах при атмосферном давлении расстояния между молекулами много больше размера самих молекул. В связи с этим притяжение молекул газа мало. Средняя кинетическая энергия молекул газа вполне достаточна, чтобы совершить работу по преодолению сил молекулярного притяжения. Поэтому, если газу не мешают стенки сосуда, его молекулы разлетаются.
В жидкостях и твёрдых телах, плотность которых во много раз больше плотности газа, молекулы расположены ближе друг к другу. Средняя кинетическая энергия их уже недостаточна для того, чтобы совершить работу по преодолению сил молекулярного притяжения.
а)
б)
в)

В каких агрегатных состояниях может находиться одно и то же вещество? 2. Какое практическое значение имеют явления перехода вещества из одного агрегатного состояния в другое? 3 Чем определяется то или иное агрегатное состояние вещества? 4. Каковы особенности молекулярного строения газов, жидкостей и твёрдых тел?

Плавление олова в стальной ложке

Одни кристаллические тела плавятся при низкой температуре, другие — при высокой. Лёд, например, можно расплавить, внеся его в комнату. Кусок олова или свинца — в стальной ложке, нагревая её на спиртовке. Железо плавят в специальных печах, где достигается высокая температура.
Из таблицы 3 видно, в каких широких пределах лежат температуры плавления различных веществ.
Температуру, при которой вещество плавится, называют температурой плавления вещества.


Переход вещества из твёрдого состояния в жидкое называют плавлением.
Чтобы расплавить тело, нужно сначала нагреть его до определённой температуры.
Передавая телу энергию, можно перевести его из твёрдого состояния в жидкое (например, расплавить лёд), а из жидкого — в газообразное (превратить воду в пар).
Если газ отдаёт энергию, то может превратиться в жидкость, а жидкость, отдавая энергию, может превратиться в твёрдое тело.
Поэтому молекулы в жидкостях и особенно в твёрдых телах не могут далеко удаляться друг от друга.
Таблица 3. Температура плавления некоторых веществ (при нормальном атмосферном давлении)
|
Вещество |
tпл, °С |
Вещество |
tпл, °С |
Вещество |
tпл, °С |
|
Водород |
-259 |
Натрий |
98 |
Золото |
1064 |
|
Кислород |
-219 |
Олово |
232 |
Медь |
1085 |
|
Азот |
-210 |
Свинец |
327 |
Чугун |
1200 |
|
Спирт |
-114 |
Янтарь |
360 |
Сталь |
1500 |
|
Ртуть |
-39 |
Цинк |
420 |
Железо |
1539 |
|
Лёд |
0 |
Алюминий |
660 |
Платина |
1772 |
|
Цезий |
29 |
Серебро |
962 |
Осмий |
3045 |
|
Калий |
63 |
Латунь |
1000 |
Вольфрам |
3387 |

1 Какой процесс называют плавлением?
2 Какой процесс называют отвердеванием?
3. Как называют температуру, при которой вещество плавится и отвердевает?
Например, температура плавления металла цезия 29 °С, т. е. его можно расплавить в тёплой воде.
Опыт показывает, что вещества отвердевают при той же температуре, при которой плавятся. Например, вода кристаллизуется (а лёд плавится) при 0 °С, чистое железо плавится и кристаллизуется при температуре 1539 °С.
Температура, при которой вещество отвердевает (кристаллизуется), называют температурой отвердевания или кристаллизации.
Чтобы началась кристаллизация расплавленного тела, оно должно остыть до определённой температуры.
Переход вещества из жидкого состояния в твёрдое называют отвердеванием или кристаллизацией.
1. Будет ли плавиться свинец, если его бросить в расплавленное олово? Ответ обоснуйте.
2. Можно ли в алюминиевом сосуде расплавить цинк? Ответ обоснуйте.
3. Почему для измерения температуры наружного воздуха в холодных районах применяют термометры со спиртом, а не с ртутью?
Какой из металлов, приведённых в таблице 3, самый легкоплавкий; самый тугоплавкий?
2. Сравните температуры плавления твёрдой ртути и твёрдого спирта. У какого из этих веществ температура плавления выше?
Плавление кристаллического тела — сложный процесс. Для его изучения рассмотрим график зависимости температуры кристаллического тела (льда) от времени его нагревания (рис. 18). На нём по горизонтальной оси отложено время, а по вертикальной — температура льда.
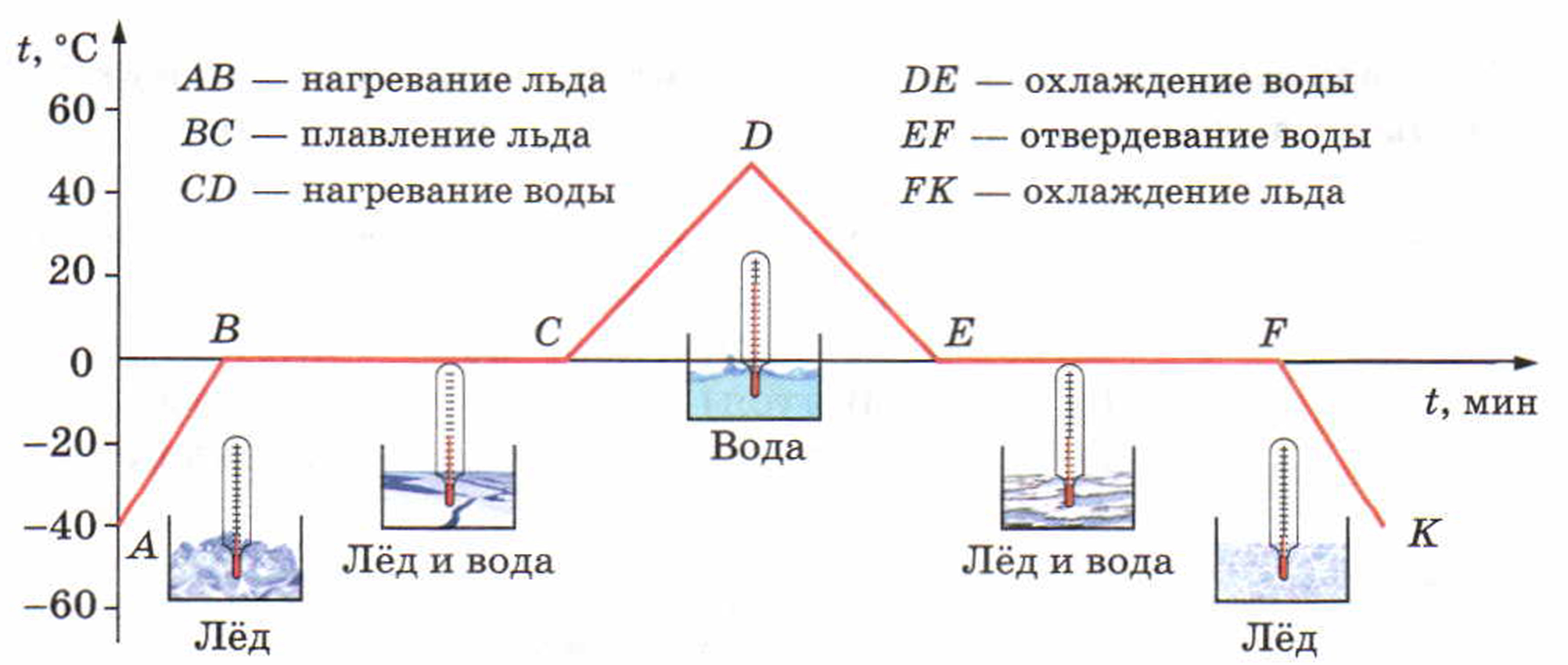
Рис. 18. График зависимости температуры льда от времени нагревания




Из графика видно, что наблюдение за процессом началось с момента, когда температура льда была -40 °С. При дальнейшем нагревании температура льда росла. На графике это участок АВ. Увеличение температуры происходило до 0 °С — температуры плавления льда. При 0 °С лёд начал плавиться, а его температура перестала расти. В течение всего времени плавления температура льда не менялась, хотя горелка продолжала гореть. Этому процессу соответствует горизонтальный участок графика — ВС.
После того как весь лёд расплавился и превратился в воду, температура снова стала подниматься (участок CD). Когда температура достигла +40 °С (точка D), горелка была погашена. Как видно из графика, температура воды после этого начала снижаться (участок DE). Вода стала охлаждаться. Когда её температура упала до 0 °С, начался процесс отвердевания воды — её кристаллизация, и пока вся вода не отвердеет, температура её не изменится (участок EF). Лишь после этого температура твёрдой воды — льда стала уменьшаться (участок FK).
Начертите график плавления меди. По вертикали отложите температуру (1 клетка — 20 °С), а по горизонтали — время (1 клетка — 10 мин). Начальная температура меди равна 1000 °С, время нагревания до температуры плавления 20 мин, время перехода меди в жидкое состояние 30 мин.
1. Пользуясь графиком (см. рис. 18) и текстом, относящимся к нему, объясните, что происходит с водой в отрезки времени, соответствующие каждому из участков графика. 2. Как по графику можно судить об изменении температуры вещества при нагревании и охлаждении? 3. Какие участки графика соответствуют плавлению и отвердеванию льда? Почему эти участки параллельны оси времени?

Это любопытно...
Аморфные тела. Плавление аморфных тел
Существует особый вид тел, который принято также называть твёрдыми телами. Это аморфные тела. В естественных условиях они не обладают правильной геометрической формой.
К аморфным телам относятся: твёрдая смола (вар, канифоль), стекло, сургуч, эбонит, различные пластмассы.
По многим физическим свойствам, да и по внутреннему строению аморфные тела стоят ближе к жидкостям, чем к твёрдым телам.
Кусок твёрдой смолы от удара рассыпается на осколки, т. е. ведёт себя как хрупкое тело, но вместе с тем обнаруживает и свойства, присущие жидкостям. Твёрдые куски смолы, например, медленно растекаются по горизонтальной поверхности, а находясь в сосуде, со временем принимают его форму. По описанным свойствам твёрдую смолу можно рассматривать как очень густую и вязкую жидкость.
Стекло обладает значительной прочностью и твёрдостью, т. е. свойствами, характерными для твёрдого тела. Однако стекло, хотя и очень медленно, способно течь, как смола.
В отличие от кристаллических тел, в аморфных телах атомы или молекулы расположены беспорядочно, как в жидкостях.
Кристаллические твёрдые тела, как мы видели (см. рис. 18), плавятся и отвердевают при одной и той же строго определённой для каждого вещества температуре. Иначе ведут себя аморфные вещества, например смола, воск, стекло. При нагревании они постепенно размягчаются, разжижаются и, наконец, превращаются в жидкость. Температура их при этом изменяется непрерывно. При отвердевании аморфных тел температура их также понижается непрерывно.
В аморфных твёрдых телах, как и в жидкостях, молекулы могут свободно перемещаться друг относительно друга. При нагревании аморфного тела скорость движения молекул увеличивается, увеличиваются расстояния между молекулами, а связи между ними ослабевают. В результате аморфное тело размягчается, становится текучим.
Зная строение аморфных тел, можно создавать материалы с заданными свойствами. В последние годы аморфные тела находят широкое применение при производстве считывающих головок аудио- и видеомагнитофонов, устройств записи и хранения информации в компьютерной технике, магнитных экранов и др.

Аморфное тело — смола

Переход металла в жидкое состояние при нагревании его до температуры плавления

В предыдущем параграфе мы рассматривали график плавления и отвердевания льда. Из графика видно, что, пока лёд плавится, температура его не меняется (см. рис. 18). И лишь после того, как весь лёд расплавится, температура образовавшейся жидкости начинает повышаться. Но ведь и во время процесса плавления лёд получает энергию от сгорающего в нагревателе топлива. А из закона сохранения энергии следует, что она не может исчезнуть. На что же расходуется энергия топлива во время плавления?
Мы знаем, что в кристаллах молекулы (или атомы) расположены в строгом порядке. Однако и в кристаллах они находятся в тепловом движении (колеблются). При нагревании тела средняя скорость движения молекул возрастает. Следовательно, возрастает и их средняя кинетическая энергия и температура. На графике это участок АВ (см. рис. 18). Вследствие этого размах колебаний молекул (или атомов) увеличивается. Когда тело нагреется до температуры плавления, то нарушится порядок в расположении частиц в кристаллах. Кристаллы теряют свою форму. Вещество плавится, переходя из твёрдого состояния в жидкое.
Следовательно, вся энергия, которую получает кристаллическое тело после того, как оно уже нагрето до температуры плавления, расходуется на разрушение кристалла. В связи с этим температура тела перестаёт повышаться. На графике (см. рис. 18) это участок ВС.
Опыты показывают, что для превращения различных кристаллических веществ одной и той же массы в жидкость при температуре плавления требуется разное количество теплоты.
Физическая величина, показывающая, какое количество теплоты необходимо сообщить кристаллическому телу массой 1 кг, чтобы при температуре плавления полностью перевести его в жидкое состояние, называется удельной теплотой плавления.

Удельную теплоту плавления обозначают λ (греч. буква «лямбда»). Её единица Дж/кг.
Определяют удельную теплоту плавления на опыте. Так, было установлено, что удельная теплота плавления льда равна 3,4 • 105 — . Это означает, что для превращения куска льда массой 1 кг, взятого при 0 °С, в воду такой же температуры требуется затратить 3,4 • 105 Дж энергии. А чтобы расплавить брусок из свинца массой 1 кг, взятого при его температуре плавления, потребуется затратить 2,5 • 104 Дж энергии.
Следовательно, при температуре плавления внутренняя энергия вещества в жидком состоянии больше внутренней энергии такой же массы вещества в твёрдом состоянии.
Чтобы вычислить количество теплоты Q, необходимое для плавления кристаллического тела массой т, взятого при его температуре плавления и нормальном атмосферном давлении, нужно удельную теплоту плавления к умножить на массу тела т:
Q = кт.
Из этой формулы можно определить, что
к — —, т — ^.
т /.
Опыты показывают, что при отвердевании кристаллического вещества выделяется точно такое же количество теплоты, которое поглощается при его плавлении. Так, при отвердевании воды массой 1 кг при температуре О °С выделяется количество теплоты, равное 3,4 • 105 Дж. Точно такое же количество теплоты требуется и для плавления льда массой 1 кг при температуре О °С.
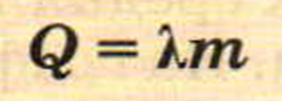
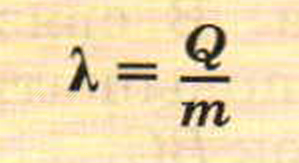
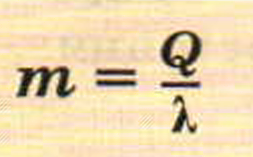
При отвердевании вещества всё происходит в обратном порядке. Скорость, а значит, и средняя кинетическая энергия молекул в охлаждённом расплавленном веществе уменьшаются. Силы притяжения теперь могут удерживать медленно движущиеся молекулы друг около друга. Вследствие этого расположение частиц становится упорядоченным — образуется кристалл. Выделяющаяся при кристаллизации энергия расходуется на поддержание постоянной температуры. На графике это участок EF (см. рис. 18).
Кристаллизация облегчается, если в жидкости с самого начала присутствуют какие-либо посторонние частицы, например пылинки. Они становятся центрами кристаллизации. В обычных условиях в жидкости имеется множество центров кристаллизации, около которых и происходит образование кристалликов.
|
Вещество |
Дж/кг |
Вещество |
Дж/кг |
|
Алюминий |
3,9-105 |
Сталь |
0,84 -105 |
|
Лёд |
3,4-105 |
Золото |
0,67-105 |
|
Железо |
2,7-105 |
Водород |
0,59-105 |
|
Медь |
2,1 • 105 |
Олово |
0,59-105 |
|
Парафин |
1,5 -105 |
Свинец |
0,25-105 |
|
Спирт |
1,1-105 |
Кислород |
0,14-105 |
|
Серебро |
0,87-105 |
Ртуть |
0,12-105 |
При кристаллизации происходит выделение энергии и передача её окружающим телам.
Количество теплоты, выделяющееся при кристаллизации тела массой т, определяется также по формуле
Q = кт.
Внутренняя энергия тела при этом уменьшается.

Таблица 4. Удельная теплота плавления некоторых веществ (при нормальном атмосферном давлении)

Пример. Для приготовления чая турист положил в котелок лёд массой 2 кг, имеющий температуру О °С. Какое количество теплоты необходимо для превращения этого льда в кипяток при температуре 100 °С? Энергию, израсходованную на нагревание котелка, не учитывать.
Какое количество теплоты понадобилось бы, если вместо льда турист взял из проруби воду той же массы при той же температуре?
Запишем условие задачи и решим её.
Нагревание льда в котелке

Нагревание льда в котелке
Дано: Решение:
т = 2 кг ЛёД прежде всего должен
t = q 0£ расплавиться, а для этого
1 потребуется количество
t =1 по °Г
t-2 теплоты:
Х = 3,4*105— Ql = Xm,
кг 1
с = 4 2 • 103 Дж Q, = 3,4-Ю5 3^-2 кг =
’ кг • °С 1 кг
= 6,8*105Дж.
Q — ? Для нагревания получен
ной изо льда воды от 0 до 100 °С потребуется количество теплоты:
Q2 = cm{t2 - tx),
Q2 = 4,2 • 103 -Щ- • 2 кг (100 °C - 0 °C) =
КГ • Ks
= 8,4 • 105 Дж.
Общее количество теплоты:
Q — Qi + Q2,
Q = 6,8 • 105 Дж + 8,4 • 105 Дж =
= 15,2 • 105 Дж.
Если бы вместо льда была взята вода массой 2 кг при температуре 0 °С, то понадобилось бы количество теплоты, необходимое только для её нагревания от 0 до 100 °С, т. е. Q2 = = 8,4 • 105 Дж.
Ответ: Q = 15,2 • 105 Дж.
Как объяснить процесс плавления тела на основе учения о строении вещества? На что расходуется энергия топлива при плавлении кристаллического тела, нагретого до температуры плавления?
3. Что называется удельной теплотой плавления? 4. Как объяснить процесс отвердевания на основе учения о строении вещества? 5. Как вычисляют количество теплоты, необходимое для плавления кристаллического тела, взятого при температуре плавления? 6. Как вычислить количество теплоты, выделяющееся при кристаллизации тела, имеющего температуру плавления?
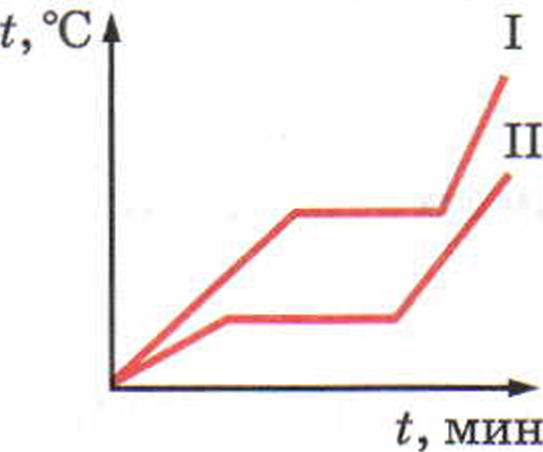
Рис. 19

1. Поставьте на плиту две одинаковые жестяные банки. В одну налейте воду массой 0,5 кг, в другую положите несколько кубиков льда той же массы. Заметьте, сколько времени потребуется, чтобы вода в обеих банках закипела. Напишите краткий отчёт о вашем опыте и объясните его результаты.
2. Прочитайте параграф «Аморфные тела. Плавление аморфных тел». Подготовьте по нему доклад.

1. На рисунке 19 изображены графики зависимости температуры от времени двух тел одинаковой массы. У какого из тел выше температура плавления? У какого тела больше удельная теплота плавления? Одинаковы ли удельные теплоёмкости тел?
2. Тающий лёд принесли в помещение, температура которого 0 °С. Будет ли лёд в этом помещении продолжать таять?
3. В ведре с водой плавают куски льда. Общая температура воды и льда 0 °С. Будет ли лёд таять или вода замерзать? От чего это зависит?
4. Сколько энергии нужно затратить, чтобы расплавить лёд массой 4 кг при температуре 0 °С?
5. Сколько энергии требуется затратить, чтобы расплавить свинец массой 20 кг при температуре плавления? Сколько энергии понадобится для этого, если начальная температура свинца 27 °С?

Из повседневных наблюдений известно, что количество воды, эфира, бензина и другой жидкости, которая находится в открытом сосуде, постепенно уменьшается. На самом деле жидкость не может исчезнуть бесследно, она превращается в пар.
Мы знаем, что молекулы жидкости непрерывно движутся с разными скоростями. Если какая-нибудь достаточно «быстрая» молекула окажется у поверхности жидкости, то она может преодолеть притяжение соседних молекул и вылететь из жидкости. Вылетевшие с поверхности жидкости молекулы образуют над ней пар. У оставшихся молекул жидкости при соударениях меняются скорости. Некоторые из молекул приобретают при этом скорость, достаточную для того, чтобы, оказавшись у поверхности, вылететь из жидкости. Этот процесс продолжается, поэтому жидкость испаряется постепенно.
Скорость испарения зависит от нескольких причин.
Если листок бумаги смочить в одном месте эфиром, а в другом водой, то мы заметим, что эфир испарится значительно быстрее, чем вода. Значит, скорость испарения зависит от рода жидкости. Быстрее испаряется та жидкость, молекулы которой притягиваются друг к другу с меньшей силой. Ведь в этом случае преодолеть притяжение и вылететь из жидкости может большее число молекул.
Так как некоторое число быстро движущихся молекул всегда имеется в жидкости, то
Парообразование, происходящее с поверхности жидкости, называется испарением.
Явление превращения жидкости в пар называется парообразованием.
Существует два способа перехода жидкости в газообразное состояние: испарение и кипение.



Испарение воды
Обмеление Аральского моря в результате потери воды при испарении и резком понижении притока внешних вод
испарение должно происходить при любой температуре. Наблюдения подтверждают это. Например, лужи, образовавшиеся после дождя, высыхают и летом в жару, и осенью, когда уже холодно. Но летом они высыхают быстрее. Дело в том, что чем выше температура жидкости, тем больше в ней быстро движущихся молекул. Они способны преодолеть силы притяжения окружающих молекул и вылететь с поверхности жидкости.
Поэтому испарение происходит тем быстрее, чем выше температура жидкости.
Если в узкий и широкий сосуды налить по одинаковому объёму воды, то можно заметить, что в широком сосуде вода испарится значительно быстрее. Например, вода, налитая в блюдце, испаряется быстрее, чем вода, налитая в стакан. Развешанное бельё быстрее высыхает, чем скомканное. Это объясняется тем, что жидкость испаряется с поверхности, и чем больше площадь поверхности жидкости, тем большее число молекул одновременно вылетает в воздух.
Значит, скорость испарения жидкости зависит от площади её поверхности.
Одновременно с переходом молекул из жидкости в пар происходит и обратный процесс. Беспорядочно двигаясь над поверхностью жидкости, часть молекул, покинувших её, снова возвращается в жидкость.
Если испарение жидкости происходит в закрытом сосуде, то вначале число молекул, вылетевших из жидкости, будет больше числа молекул, возвратившихся обратно в жидкость. Поэтому плотность пара в сосуде будет постепенно увеличиваться. С увеличением плотности пара увеличится и число молекул, возвращающихся в жидкость. Довольно скоро число молекул, вылетающих из жидкости, станет равным числу молекул пара, возвращающихся обратно в жидкость. С этого момента число молекул пара над жидкостью будет постоянным.

При динамическом равновесии масса жидкости в закрытом сосуде не изменяется, хотя жидкость продолжает испаряться (рис. 20).
В открытом сосуде масса жидкости вследствие испарения постепенно уменьшается. Это связано с тем, что большинство молекул пара рассеивается в воздухе, не возвращаясь в жидкость. Но небольшая часть их возвращается обратно в жидкость, замедляя тем самым испарение. Поэтому при ветре, который уносит молекулы пара, испарение жидкости происходит быстрее.
Зная, от каких причин зависит скорость испарения, мы можем объяснить теперь, зачем, например, переливают чай из стакана в блюдце, дуют на горячий суп или кашу, обмахиваются веером.
Наблюдения и опыты показывают, что испаряются и твёрдые тела. Испаряется, например, лёд, поэтому бельё высыхает и на морозе. Испаряется нафталин, поэтому мы чувствуем его запах.
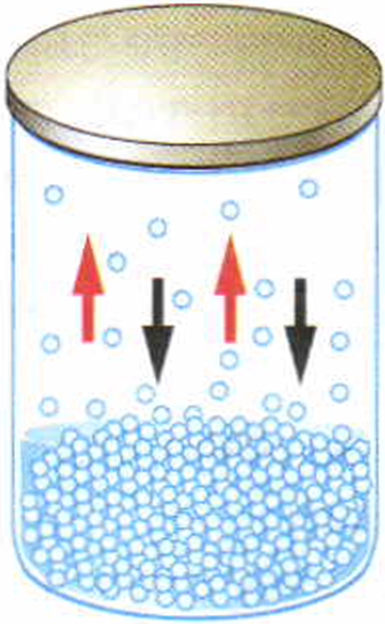
Рис. 20. Испарение жидкости в закрытом сосуде
1. Какое явление называют испарением? 2. Почему испарение жидкости происходит при любой температуре? 3. От чего зависит скорость испарения жидкости? 4. Почему испарение происходит тем
Наступает так называемое динамическое равновесие между паром и жидкостью.
Пар, находящийся в динамическом равновесии со своей жидкостью, называется насыщенным.
Если в пространстве, содержащем пары какой-либо жидкости, может происходить дальнейшее испарение этой жидкости, то пар, находящийся в этом пространстве, является ненасыщенным паром.
Пар, не находящийся в состоянии равновесия со своей жидкостью, называется ненасыщенным.



быстрее, чем выше температура жидкости? 5. Как зависит скорость испарения жидкости от площади её поверхности? 6. Какой пар называется насыщенным? 7. Какой пар называется ненасыщенным? 8. Почему испарение жидкости происходит быстрее, если над её поверхностью дует ветер?
1. На стеклянную пластинку или блюдце с помощью пипетки капните по 1—2 капли воды, масла и духов. Пронаблюдайте, какая капля испарится первой, а какая последней. Дайте объяснение.
2. Возьмите корректирующую жидкость на водной основе. Нанесите её на две буквы, написанные на разных листах. На одну из букв, покрытую корректирующей жидкостью, подуйте. Объясните, почему в последнем случае она высохнет быстрее.

Конденсация пара на окне
При испарении жидкость покидают наиболее быстрые молекулы, поэтому средняя скорость остальных молекул жидкости становится меньше. Следовательно, и средняя кинетическая энергия остающихся в жидкости молекул уменьшается. Это означает, что внутренняя энергия испаряющейся жидкости уменьшается. Поэтому, если нет притока энергии к жидкости извне, испаряющаяся жидкость охлаждается.
Охлаждение жидкости при испарении можно наблюдать на опыте. Для этого нужно обмотать шарик термометра ватой (или кусочком материи) и полить её эфиром. Быстро испаряющийся эфир отнимает часть внутренней энергии от шарика термометра, вследствие чего температура последнего понижается. Если эфиром смочить руку, то мы будем ощущать охлаждение.



Выпадение росы
Выходя из воды даже в жаркий день, мы чувствуем, что нам прохладно. Вода, испаряясь с поверхности нашего тела, отнимает от него некоторое количество теплоты.

Однако при испарении воды, налитой в стакан, мы не замечаем понижения её температуры. Чем это объяснить? Дело в том, что испарение в данном случае происходит медленно и температура воды поддерживается постоянной за счёт количества теплоты, поступающего из окружающего воздуха. Значит, чтобы испарение жидкости происходило без изменения её температуры, жидкости необходимо сообщать энергию. Испарение жидкости сопровождается поглощением энергии.
Испарение имеет большое значение в жизни животных. Затруднение испарения нарушает теплоотдачу и может вызвать перегревание тела.
Известно, что одновременно с испарением происходит переход молекул из пара в жидкость.
Явление превращения пара в жидкость называется конденсацией.
Термин «конденсация» происходит от латинского слова конденсаре — «сгущать».
Конденсация пара сопровождается выделением энергии.
Летним вечером, когда воздух становится холоднее, выпадает роса. Это водяной пар, находившийся в воздухе, при охлаждении конденсируется, и маленькие капельки воды оседают на траве и листьях.
Конденсацией пара объясняется образование облаков. Пары воды, поднимающиеся над землёй, образуют в верхних, более холодных слоях воздуха облака, состоящие из мельчайших капелек воды.
1. Против каких сил совершают работу молекулы, выходящие из жидкости при испарении? 2. Как объяснить понижение температуры жидкости при её испарении? 3. Как можно на опыте показать охлаждение жидкости при испарении? 4. Как можно объяснить, что при одних и тех же условиях одни жидкости испаряются быстрее, другие — медленнее? 5. При каких условиях происходит конденсация пара? 6. Какие явления природы объясняются конденсацией пара? Приведите примеры и объясните их.

1. В какую погоду скорее просыхают лужи от дождя: в тихую или ветреную; в тёплую или холодную? Как это можно объяснить?
2. Почему горячий чай остывает быстрее, если на него дуют?
3. Выступающий в жару на теле пот охлаждает тело. Почему?
4. Почему в сухом воздухе переносить жару легче, чем во влажном?
5. Чтобы остудить воду в летнюю жару, её наливают в сосуды, изготовленные из слабообожжённой глины, сквозь которую вода медленно просачивается. Вода в таких сосудах холоднее окружающего воздуха. Почему?
6. В блюдце и в стакан налита вода одинаковой массы. Где вода быстрее испарится? Почему?
Для чего летом после дождей или полива приствольные круги плодовых деревьев покрывают слоем перегноя, навоза или торфа?

В два одинаковых блюдца налейте по одинаковому количеству воды (например, по три столовых ложки). Одно блюдце поставьте в тёплое место, а другое — в холодное. Запишите, за какое время испарится вода в том и другом блюдце. Объясните разницу в скорости испарения.


Кипение воды
Рассмотрим второй способ образования пара — кипение.
Пронаблюдаем это явление на опыте. Для этого будем нагревать воду в открытом стеклянном сосуде, измеряя её температуру. Прежде всего обратим внимание на то, что с поверхности воды происходит испарение. На это указывает туман, образовавшийся над сосудом.
Это водяной пар смешивается с холодным воздухом и конденсируется в виде маленьких капель. Сам пар, конечно, невидим глазу.
При дальнейшем повышении температуры мы заметим появление в воде многочисленных мелких пузырьков (рис. 21, а). Они постепенно увеличиваются в размерах. Это пузырьки воздуха, который растворён в воде. При нагревании воздух выделяется из воды в виде пузырьков. Эти пузырьки содержат не только воздух, но и водяной пар, так как вода испаряется внутрь этих пузырьков воздуха. Поднимающиеся пузырьки, попадая в верхние, более холодные слои воды, уменьшаются в размерах, так как содержащиеся в них пары конденсируются и под действием силы тяжести они опускаются. Спустившись ниже, в более горячие слои воды, пузырьки начинают снова подниматься к поверхности. Это попеременное увеличение и уменьшение пузырьков в размерах сопровождается характерным шумом, предшествующим закипанию воды. Постепенно вся вода прогревается, пузырьки уже не уменьшаются в размерах. Под действием архимедовой силы они всплывают на поверхность и лопаются (рис. 21,6). Находящийся в них насыщенный пар выходит в атмосферу. Шум прекращается, и мы слышим бульканье — вода закипела.
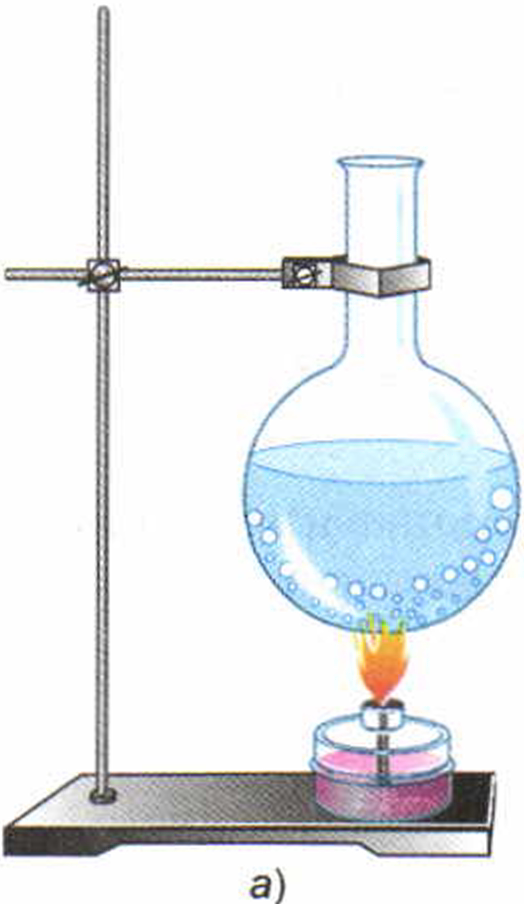
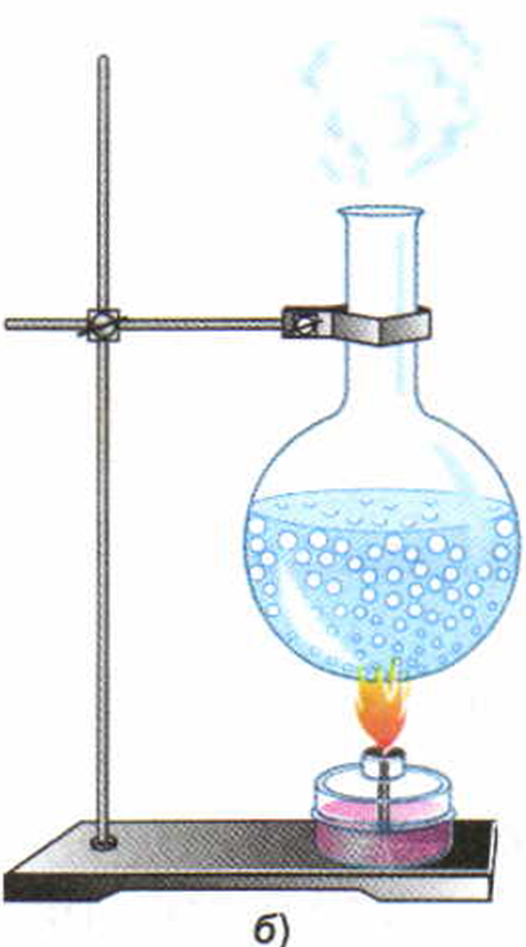
Рис. 21. Нагревание воды
Следует помнить, что у различных жидкостей температура кипения разная (табл. 5).
В отличие от испарения, которое происходит при любой температуре (см. § 17), кипение от начала до конца происходит при определённой и постоянной для каждой жидкости температуре. Поэтому, например, при варке пищи нужно уменьшать огонь после того, как вода
Кипение — это интенсивный переход жидкости в пар, происходящий с образованием пузырьков пара по всему объёму жидкости при определённой температуре.
Во время кипения температура жидкости не меняется.
Температура кипения жидкости зависит от давления, которое оказывается на поверхность жидкости. При кипении давление насыщенного пара внутри пузырьков превосходит внешнее давление. Если внешнее давление увеличивается, увеличивается и температура кипения. При уменьшении давления уменьшается и температура кипения жидкости.
Вам известно, что давление воздуха уменьшается с увеличением высоты над уровнем моря. Следовательно, с увеличением высоты уменьшается и температура кипения жидкости. Так, в горах вода закипает при £ = 90 °С. При низкой температуре кипения невозможно сварить обычное яйцо, так как белок не может свернуться, если температура ниже 100 °С.
|
Вещество |
*к„п> °С |
Вещество |
t °С кип* ^ |
|
Водород |
-253 |
Вода |
100 |
|
Кислород |
-183 |
Ртуть |
357 |
|
Молоко |
100 |
Свинец |
1740 |
|
Эфир |
35 |
Медь |
2567 |
|
Спирт |
78 |
Железо |
2750 |
Некоторые вещества, которые в обычных условиях являются газами, при достаточном охлаждении обращаются в жидкости, кипящие
Таблица 5. Температура кипения некоторых веществ (при нормальном атмосферном давлении)
Температуру, при которой жидкость кипит, называют температурой кипения.
закипит. Это даст экономию топлива, а температура воды всё равно сохраняется постоянной во время кипения.

а

при очень низкой температуре. Жидкий кислород, например, при атмосферном давлении кипит при температуре -183 °С. Вещества, которые в обычных условиях мы наблюдаем в твёрдом состоянии, обращаются при плавлении в жидкости, кипящие при очень высокой температуре. Например, медь кипит при 2567 °С, а железо — при 2750 °С.
1 Какие явления наблюдаются в жидкости перед тем, как она начинает кипеть? Какие силы действуют на пузырёк воздуха, наполненный паром, когда он находится внутри жидкости? Что называют температурой кипения жидкости?

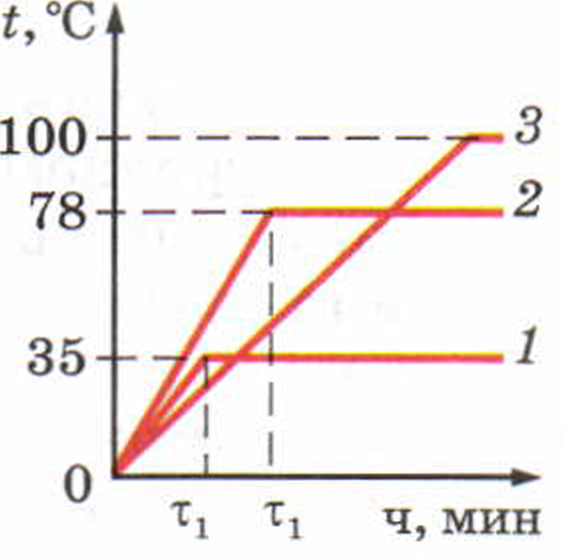
Рис. 22
1. На рисунке 22 показаны графики зависимости температуры от времени при нагревании и кипении воды, спирта и эфира. Массы жидкостей одинаковы, нагреватели одинаковой мощности. Определите, какой жидкости соответствуют графики 1,2,3.
Нагреется ли вода до более высокой температуры, если её дольше кипятить?
Объясните, почему высоко в горах вода закипает при температуре ниже 100 °С.

Поставьте на плиту кастрюлю, наполненную водой. Опишите, что происходит с водой по мере её закипания. Объясните наблюдаемое явление.

Конденсационный гигрометр
Окружающий нас атмосферный воздух вследствие непрерывного испарения воды с поверхности водоёмов и растительных покровов всегда содержит в себе водяные пары. Содержание водяного пара в атмосфере характеризует такое понятие, как «влажность». Она имеет большое значение для многих процессов, происходящих в атмосфере. Влажность воздуха характеризует погоду и климат, влияет на теплообмен организма с окружающей средой, на жизнь животных и растений.
Чем больше водяных паров находится в определённом объёме воздуха, тем ближе пар к состоянию насыщения. С другой стороны, чем выше температура воздуха, тем большее количество водяных паров потребуется для его насыщения.
В зависимости от количества паров, находящихся при данной температуре в атмосфере, воздух бывает различной степени влажности.
Абсолютная влажность р показывает, сколько граммов водяного пара содержится в воздухе объёмом 1 м3 при данных условиях, т. е. плотность водяного пара.
Чтобы судить о степени влажности воздуха, важно знать, близок или далёк водяной пар, находящийся в воздухе, от состояния насыщения. Для этого вводят понятие относительной влажности.
Относительной влажностью воздуха ср называют отношение абсолютной влажности воздуха р к плотности р0 насыщенного водяного пара при той же температуре, выраженной в процентах.
Относительную влажность воздуха можно определить по формуле 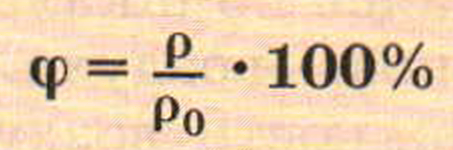
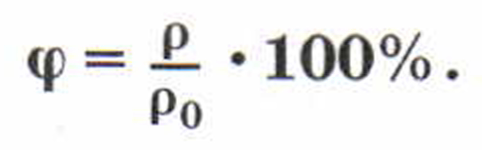
Если влажный воздух охлаждать, то при некоторой температуре находящийся в нём пар можно довести до насыщения. При дальнейшем охлаждении водяной пар начнёт конденсироваться в виде росы. Появляется туман, выпадает роса.

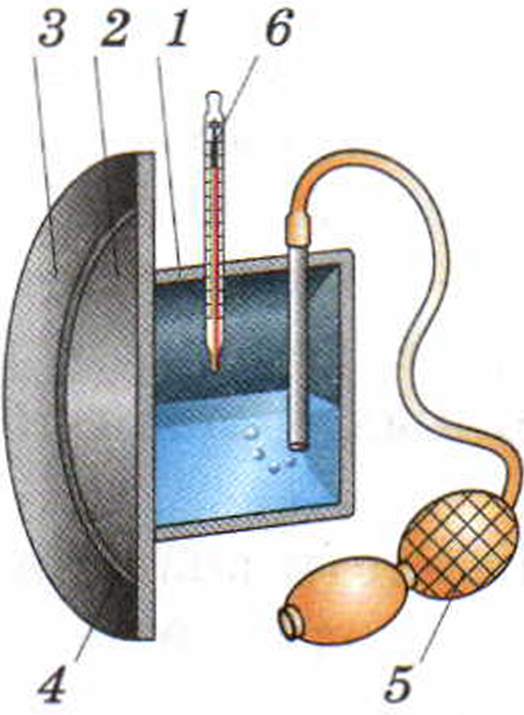
Рис. 23. Внешний вид и устройство конденсационного гигрометра

Рис. 24. Волосной гигрометр
Температура, при которой пар, находящийся в воздухе, становится насыщенным, называется точкой росы.
Точка росы также характеризует влажность воздуха.
Для определения влажности воздуха используют такие приборы, как гигрометр и психрометр.
Гигрометры бывают двух видов — конденсационные и волосные.
С помощью конденсационного гигрометра можно определить абсолютную влажность воздуха по точке росы. Он представляет собой металлическую коробочку 1 (рис. 23). Её передняя стенка 2 хорошо отполирована и окружена также отполированным кольцом 3. Между стенкой и кольцом расположена теплоизолирующая прокладка 4. К коробочке подсоединена резиновая груша 5 и вставлен термометр 6.
Если в коробку налить легко испаряющуюся жидкость (эфир), то, продувая воздух через коробку с помощью груши, можно вызвать сильное испарение эфира и быстрое охлаждение коробки. На полированной поверхности появляются капельки росы. По термометру замечают температуру, при которой они появляются. Это и есть точка росы, так как появление росы говорит о том, что пар стал насыщенным. По таблице плотности насыщенного водяного пара и определяют абсолютную влажность воздуха.
Действие волосного гигрометра (рис. 24) основано на свойстве человеческого волоса удлиняться при увеличении относительной влажности воздуха. При увеличении влажности воздуха длина волоса увеличивается, а при уменьшении влажности его длина уменьшается. При этом стрелка, перемещаясь по шкале, указывает относительную влажность воздуха.

Психрометр
Прибор для определения влажности воздуха — психрометр — состоит из двух термометров, один из которых обмотан тканью, конец которой опущен в воду. Поскольку вода испаряется, то термометр охлаждается. Чем больше относительная влажность, тем менее интенсивно идёт испарение. Следовательно, разность показаний сухого и влажного термометров будет меньше. По этой разности температур с помощью специальных таблиц и определяют относительную влажность воздуха.
Влажность воздуха меняется в течение суток. Температура воздуха днём выше, чем ночью, поэтому относительная влажность воздуха днём меньше, чем в ночное время.
Определение влажности воздуха необходимо в метеорологии для предсказания погоды, в теплицах и оранжереях для поддержания нужного режима растениям. Работа многих технических устройств и возникновение коррозии зависит от влажности воздуха. Для хранения произведений искусства и книг необходимо поддерживать влажность воздуха на определённом уровне. От влажности воздуха зависит интенсивность испарения влаги с поверхности кожи человека. Чтобы человек чувствовал себя комфортно, влажность воздуха в помещениях должна быть 40—60% .

1. Оба термометра в психрометре показывают одинаковую температуру. Какова относительная влажность воздуха?
Как изменится разность показаний сухого и влажного термометров в психрометре при понижении температуры воздуха, если абсолютная влажность остаётся без изменения?
3. Почему вечером после жаркого дня появляется роса?

Что называют относительной влажностью воздуха? Что называется точкой росы? 3. Какие приборы используют для определения влажности воздуха? 4. Как определить точку росы с помощью конденсационного гигрометра? 5. Как, используя психрометр, можно узнать относительную влажность воздуха?
Кипение, как мы видели, тоже испарение, только сопровождается оно быстрым образованием и ростом пузырьков пара. Очевидно, что во время кипения необходимо подводить к жидкости определённое количество теплоты. Это количество теплоты идёт на образование пара. Причём различные жидкости одной и той же массы требуют разное количество теплоты для обращения их в пар при температуре кипения.
Опытами было установлено, что для испарения воды массой 1 кг при температуре 100 °С требуется 2,3 • 106 Дж энергии. Для испарения эфира массой 1 кг, взятого при температуре 35 °С, необходимо 0,4 • 106 Дж энергии.
Следовательно, чтобы температура испаряющейся жидкости не изменялась, к жидкости необходимо подводить определённое количество теплоты.
Физическая величина, показывающая, какое количество теплоты необходимо, чтобы обратить жидкость массой 1 кг в пар без изменения температуры, называется удельной теплотой парообразования.
Удельную теплоту парообразования обозначают буквой L. Её единица — 1 — .КГ
Опытами установлено, что удельная теплота парообразования воды при 100 °С равна 2,3 *106 Дж/кг. Иными словами, для превращения воды массой 1 кг в пар при температуре 100 °С требуется 2,3 • 106 Дж энергии. Следовательно, при температуре кипения внутренняя энергия вещества в парообразном состоянии больше внутренней энергии такой же массы вещества в жидком состоянии.

Таблица 6. Удельная теплота парообразования некоторых веществ
(при температуре кипения и нормальном атмосферном давлении)
Рис. 25. Конденсация пара
Соприкасаясь с холодным предметом, водяной пар конденсируется (рис. 25). При этом выделяется энергия, поглощённая при образовании пара. Точные опыты показывают, что, конденсируясь, пар отдаёт то количество энергии, которое пошло на его образование.
Следовательно, при превращении 1 кг водяного пара при температуре 100 °С в воду той же температуры выделяется 2,3 • 106 Дж энергии.
Как видно из сравнения с другими веществами (табл. 6), эта энергия довольно велика.
Освобождающаяся при конденсации пара энергия может быть использована. На крупных тепловых электростанциях отработавшим в турбинах паром нагревают воду.
Нагретую таким образом воду используют для отопления зданий, в банях, прачечных и для других бытовых нужд.
Чтобы вычислить количество теплоты Q, необходимое для превращения в пар жидкости любой массы, взятой при температуре кипения, нужно удельную теплоту парообразования L умножить на массу т:
Q = Lm.
Из этой формулы можно определить, что
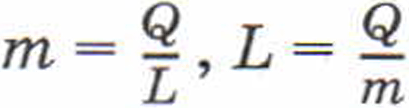
|
Вещество |
L, 3^ кг |
Вещество |
L, 3® кг |
|
Вода |
2,3 -106 |
Эфир |
0,4-106 |
|
Аммиак (жидкий) |
1,4-106 |
Ртуть |
0,3-106 |
|
Спирт |
0,9 -106 |
Воздух (жидкий) |
0,2-106 |
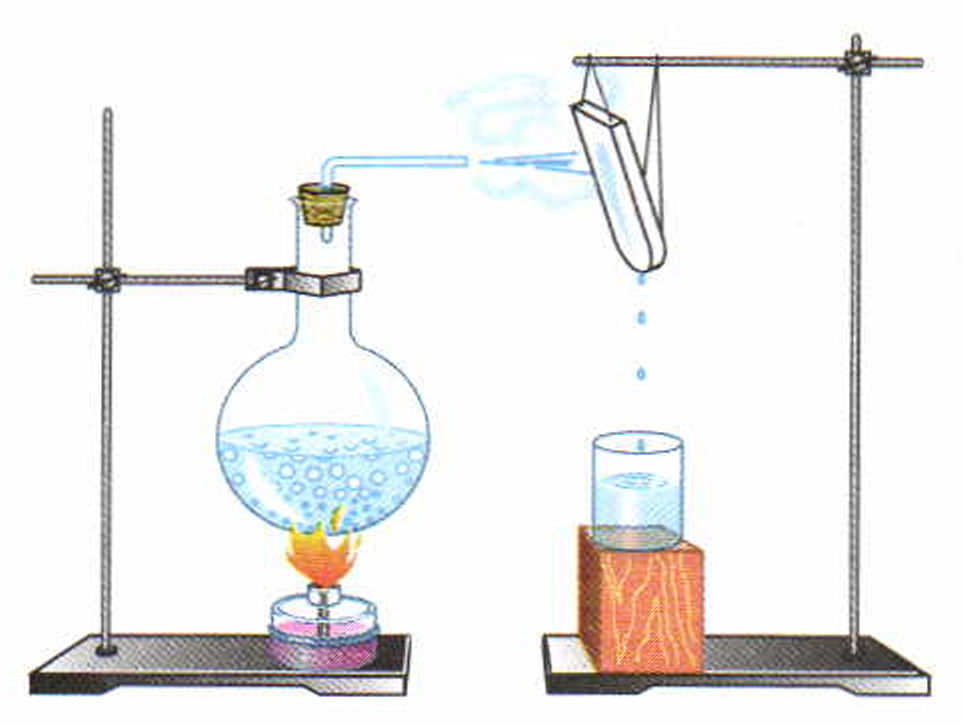
Q — Lm

Количество теплоты, которое выделяет пар массой т, конденсируясь при температуре кипения, определяется по той же формуле.
Пример. Какое количество энергии требуется для превращения воды массой 2 кг, взятой при температуре 20 °С, в пар?
Запишем условие задачи и решим её.
Дано: Решение:
т — 2 кг Общее количество израс-
t = 20 °С ходованной энергии:
t2 ~ 100 °С Q — Qj + ^2’
с = 4,2 • 103 кг. оС где Qx — энергия, кото-
дж рая необходима для на-
L = 2,3-106 —— гревания воды от 20 до
- 100°С:
? Qi = cm{t2 - £j),
a Q2 — энергия, которая необходима для превращения воды в пар без изменения её температуры:
Q2 = Lm.
Q = 4200 • 2 кг (100 °С - 20 °С) +
КГ •
+ 2,3 • 106 Й25 . 2 кг » 5,3 • 106 Дж.
КГ
Ответ: Q = 5,3 • 103 кДж.
1. На что расходуется энергия, подводимая к жидкости при кипении? 2. Что показывает удельная теплота парообразования? 3. Как можно показать на опыте, что при конденсации пара выделяется энергия? Чему равна энергия, выделяемая водяным паром массой 1 кг при конденсации? Где в технике используют энергию, выделяемую при конденсации водяного пара?

Как надо понимать, что удельная теплота парообразования воды равна 2,3 • 106 ^ ?
2. Как надо понимать, что удельная теплота конденсации аммиака равна 1,4* 106 3^?
3. У какого из приведённых в таблице 6 веществ при обращении из жидкого состояния в пар внутренняя энергия увеличивается больше? Ответ обоснуйте.
Какое количество энергии требуется для обращения воды массой 150 г в пар при температуре 100 °С?
Какое количество энергии нужно затратить, чтобы воду массой 5 кг, взятую при температуре 0 °С, довести до кипения и испарить её?
Какое количество энергии выделит вода массой 2 кг при охлаждении от 100 до 0 °С? Какое количество энергии выделится, если вместо воды взять столько же пара при 100 °С?
По таблице 6 определите, у какого из веществ при обращении из жидкого состояния в пар внутренняя энергия увеличивается сильнее. Ответ обоснуйте.
2. Подготовьте доклад на одну из тем (по выбору).
■ Как образуется роса, иней, дождь и снег.
Круговорот воды в природе.
ш Литьё металлов.
Мы уже говорили о том, что развитие техники зависит от умения использовать громадную внутреннюю энергию топлива.
Использовать внутреннюю энергию — значит совершить за счёт неё полезную работу, например поднять груз, перевезти вагоны и т. п. А это, в свою очередь, означает, что внутреннюю энергию необходимо превратить в механическую. Как это сделать?
В пробирку нальём немного воды, затем плотно закроем её пробкой и нагреем воду до кипения. Под давлением пара пробка выскочит и поднимется вверх. Здесь энергия топлива перешла во внутреннюю энергию пара, а пар, расширяясь, совершил работу — поднял пробку. Внутренняя
Шотландский инженер-изобретатель, создатель универсальной паровой машины.



Тепловой двигатель Дж. Уатта


энергия пара превратилась в кинетическую энергию пробки.
Заменим пробирку прочным металлическим цилиндром, а пробку — плотно пригнанным поршнем, который может двигаться вдоль цилиндра. Мы получим простейший тепловой двигатель, в котором внутренняя энергия топлива превращается в механическую энергию поршня. Такой двигатель был изобретён в конце XVII в. Джеймсом Уаттом и усовершенствован в дальнейшем.
Тепловыми двигателями называют машины, в которых внутренняя энергия топлива превращается в механическую энергию.
Существует несколько видов тепловых двигателей: паровая машина, двигатель внутреннего сгорания, паровая и газовая турбины, реактивный двигатель. Во всех этих двигателях энергия топлива сначала переходит в энергию газа (или пара). Газ, расширяясь, совершает работу и при этом охлаждается. Часть его внутренней энергии превращается в механическую энергию.
Из всех существующих тепловых двигателей мы рассмотрим двигатель внутреннего сгорания и паровую турбину.

Приведите примеры устройств, в которых происходит превращение внутренней энергии пара в механическую энергию. 2 Какие двигатели называют тепловыми? 3. Какие виды тепловых двигателей вам известны? Какие переходы и превращения энергии происходят в них?
ДВИГАТЕЛЬ ВНУТРЕННЕГО СГОРАНИЯ
Двигатель внутреннего сгорания — очень распространённый вид теплового двигателя. Топливо в нём сгорает прямо в цилиндре, внутри самого двигателя. Отсюда и происходит название этого двигателя.

Рис. 26. Двигатель внутреннего сгорания в разрезе
Двигатели внутреннего сгорания работают на жидком топливе (бензин, керосин, нефть) или на горючем газе.
Тепловые двигатели такого типа обычно устанавливают на автомобили.
На рисунке 26 показан простейший двигатель внутреннего сгорания в разрезе.
Двигатель состоит из цилиндра, в котором перемещается поршень 3, соединённый при помощи шатуна 4 с коленчатым валом 5.
В верхней части цилиндра имеется два клапана 1 и 2, которые при работе двигателя автоматически открываются и закрываются в нужные моменты. Через клапан 1 в цилиндр поступает горючая смесь, которая воспламеняется с помощью свечи 6, а через клапан 2 выпускаются отработавшие газы.
В цилиндре такого двигателя периодически происходит сгорание горючей смеси, состоящей из паров бензина и воздуха. Температура газообразных продуктов сгорания достигает 1600—1800 °С. Давление на поршень при этом резко возрастает.
Расширяясь, газы толкают поршень, а вместе с ним и коленчатый вал, совершая механическую работу. При этом они охлаждаются, так как часть внутренней энергии газов превращается в механическую энергию.
Рассмотрим более подробно схему работы такого двигателя. Крайние положения поршня в цилиндре называют мёртвыми точками. Расстояние, проходимое поршнем от одной мёртвой точки до другой, называют ходом поршня.
Один рабочий цикл в двигателе происходит за четыре хода поршня, или, как говорят, за четыре такта. Поэтому такие двигатели называют четырёхтактными.
Один ход поршня, или один такт двигателя, совершается за пол-оборота коленчатого вала.
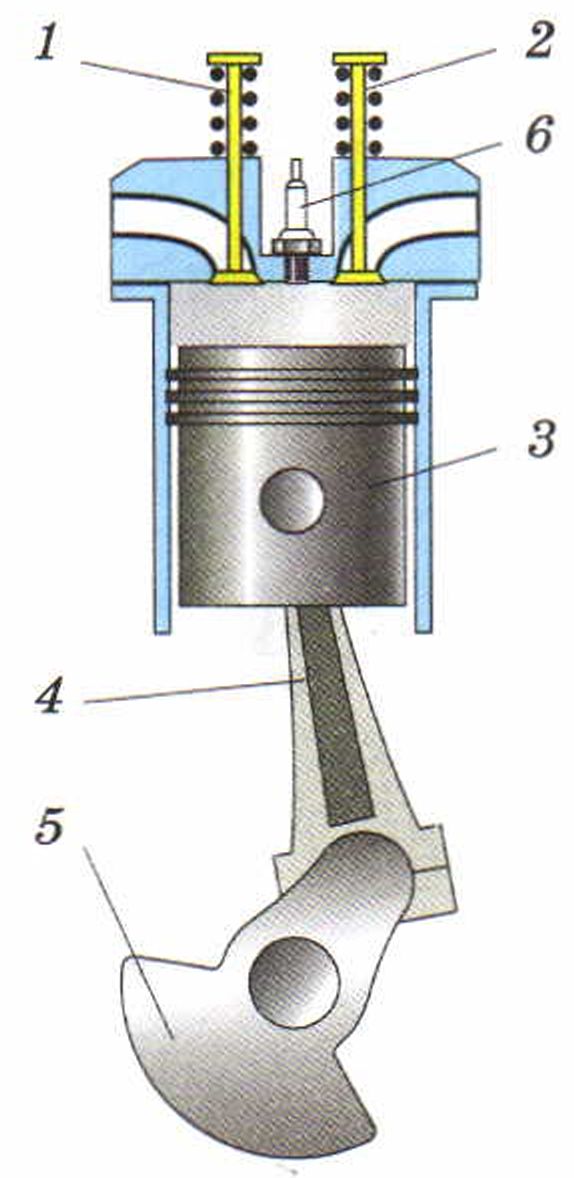
Рис. 27. Циклы работы двигателя внутреннего сгорания

в)
Двигатель внутреннего сгорания: а — мотоцикла; б — автомобиля; в — самолёта
При повороте вала двигателя в начале первого такта поршень движется вниз (рис. 27, а). Объём над поршнем увеличивается. Вследствие этого в цилиндре создаётся разрежение. В это время открывается клапан i и в цилиндр входит горючая смесь. К концу первого такта цилиндр заполняется горючей смесью, а клапан 1 закрывается.
При дальнейшем повороте вала поршень движется вверх (второй такт) и сжимает горючую смесь (рис. 27, б). В конце второго такта, когда поршень дойдёт до крайнего верхнего положения, сжатая горючая смесь воспламеняется (от электрической искры) и быстро сгорает.
Образующиеся при сгорании газы давят на поршень и толкают его вниз (рис. 27, в). Под действием расширяющихся нагретых газов (третий такт) двигатель совершает работу, поэтому этот такт называют рабочим ходом. Движение поршня передаётся шатуну, а через него коленчатому валу с маховиком. Получив сильный толчок, маховик продолжает вращаться по инерции и перемещает скреплённый с ним поршень при последующих тактах. Второй и третий такты происходят при закрытых клапанах.
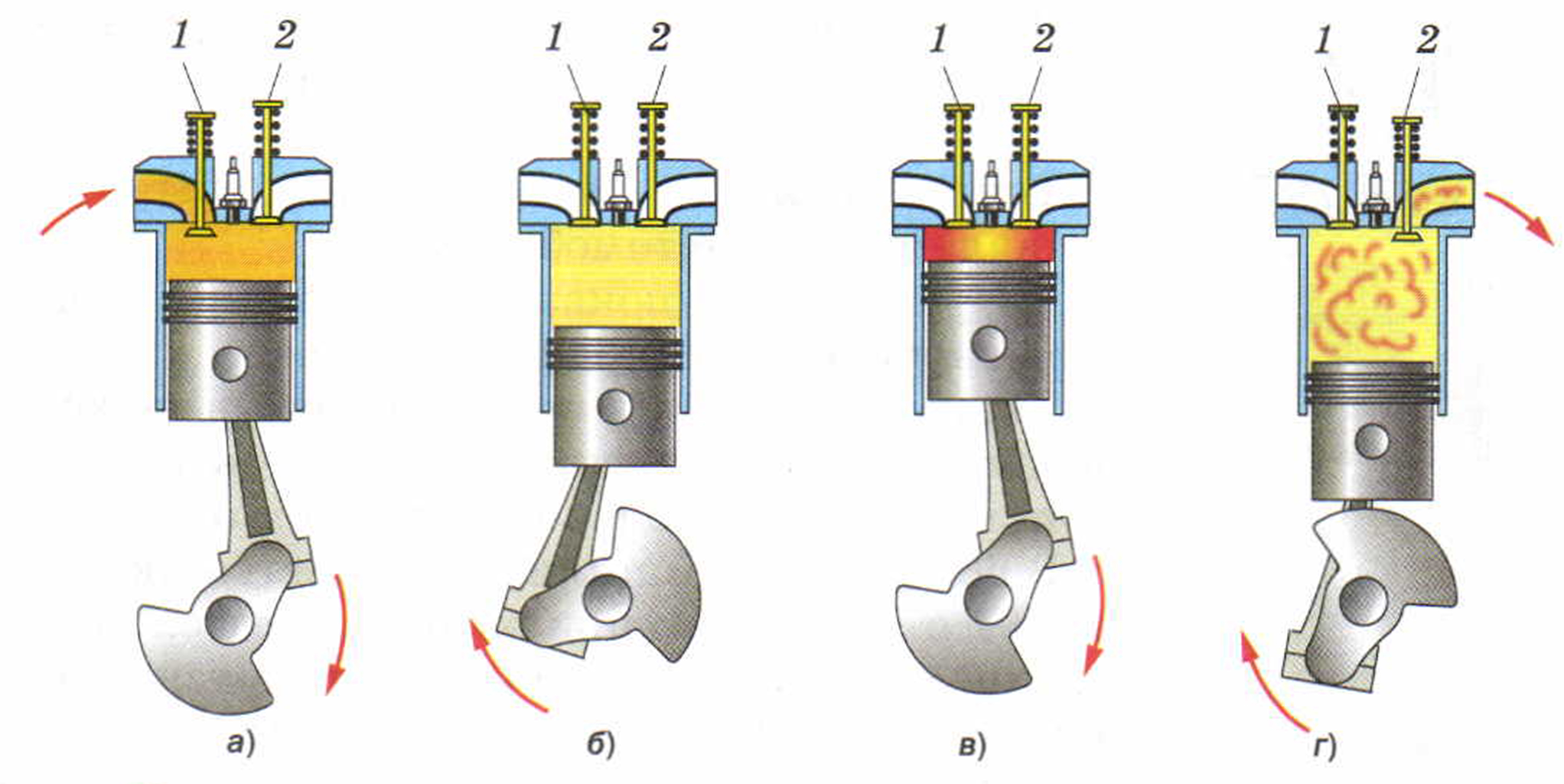

Немецкий инженер, создатель двигателя внутреннего сгорания, используемого по настоящее время.
В конце третьего такта открывается клапан 2, и через него продукты сгорания выходят из цилиндра в атмосферу. Выпуск продуктов сгорания продолжается и в течение четвёртого такта, когда поршень движется вверх (рис. 27, г). В конце четвёртого такта клапан 2 закрывается.
Итак, цикл двигателя состоит из следующих четырёх процессов {тактов): впуска, сжатия, рабочего хода, выпуска.
В автомобилях используют чаще всего четырёхцилиндровые двигатели внутреннего сгорания. Работа цилиндров согласуется так, что в каждом из них поочерёдно происходит рабочий ход и коленчатый вал всё время получает энергию от одного из поршней. Имеются и восьмицилиндровые двигатели. Многоцилиндровые двигатели в лучшей степени обеспечивают равномерность вращения вала и имеют большую мощность.
Применение двигателей внутреннего сгорания чрезвычайно разнообразно. Они приводят в движение самолёты, теплоходы, автомобили, тракторы, тепловозы. Мощные двигатели внутреннего сгорания устанавливают на речных и морских судах.
1. Какой двигатель называют двигателем внутреннего сгорания?
2. Пользуясь рисунком 26, расскажите, из каких основных частей состоит простейший двигатель внутреннего сгорания. 3. За сколько ходов, или тактов, происходит один рабочий цикл двигателя? Сколько оборотов делает при этом вал двигателя? 4. Какие процессы происходят в двигателе в течение каждого из четырёх тактов? Как называют эти такты? 5. Какую роль играет маховик в двигателе внутреннего сгорания?


Ротор паровой турбины
В современной технике широко применяют другой тип теплового двигателя. В нём пар или нагретый до высокой температуры газ вращает вал двигателя без помощи поршня, шатуна и коленчатого вала. Такие двигатели называют турбинами.
Схема устройства простейшей паровой турбины приведена на рисунке 28. На вал 5 насажен диск 4, по ободу которого закреплены лопатки 2. Около лопаток расположены трубы — сопла 1, в которые поступает пар 3 из котла. Струи пара, вырывающиеся из сопел, оказывают значительное давление на лопатки и приводят диск турбины в быстрое вращательное движение.
В современных турбинах применяют не один, а несколько дисков, насаженных на общий вал. Пар последовательно проходит через лопатки всех дисков, отдавая каждому из них часть своей энергии.
На электростанциях с турбиной соединён генератор электрического тока. Частота вращения вала турбин достигает 3000 оборотов в минуту, что является очень удобным для приведения в движение генераторов электрического тока.
В нашей стране строят паровые турбины мощностью от нескольких киловатт до 1 200 000 кВт.
Применяют турбины на тепловых электростанциях и на кораблях.
Постепенно находят всё более широкое применение газовые турбины, в которых вместо пара используются продукты сгорания газа.

Какие тепловые двигатели называют паровыми турбинами?
В чём отличие в устройстве турбин и поршневых машин?
Пользуясь рисунком 28, расскажите, из каких частей состоит паровая турбина и как она работает.

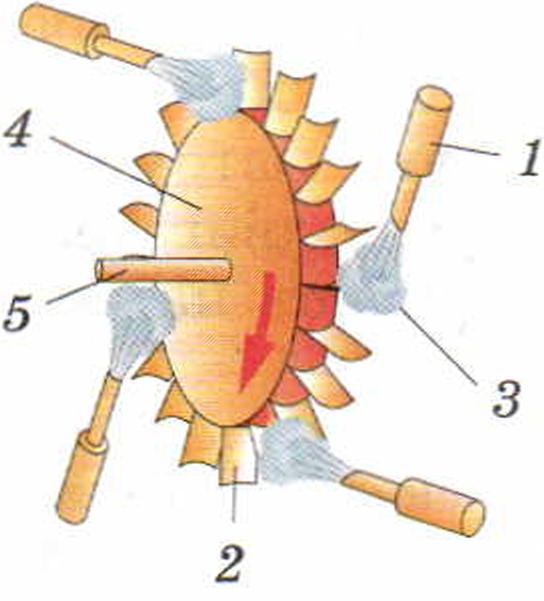
Рис. 28. Схема паровой турбины
Любой тепловой двигатель превращает в механическую энергию только незначительную часть энергии, которая выделяется топливом. Большая часть энергии топлива не используется полезно, а теряется в окружающем пространстве.
Тепловой двигатель состоит из нагревателя, рабочего тела и холодильника. Газ или пар, который является рабочим телом, получает от нагревателя некоторое количество теплоты. Рабочее тело, нагреваясь, расширяется и совершает работу за счёт своей внутренней энергии. Часть энергии передаётся атмосфере — холодильнику — вместе с отработанным паром или выхлопными газами.
Очень важно знать, какую часть энергии, выделяемой топливом, тепловой двигатель превращает в полезную работу. Чем больше эта часть энергии, тем двигатель экономичнее.
Для характеристики экономичности различных двигателей введено понятие коэффициента полезного действия двигателя — КПД.
Отношение совершённой полезной работы двигателя к энергии, полученной от нагревателя, называют коэффициентом полезного действия теплового двигателя.
Коэффициент полезного действия обозначают г\ (греч. буква «эта»).
КПД теплового двигателя определяют по формуле
,, = di, или n = • 100%,
Wi Vl
где АП — полезная работа, Ql — количество теплоты, полученное от нагревателя, Q2 — количество теплоты, отданное холодильнику,

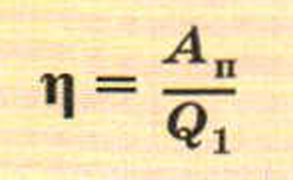
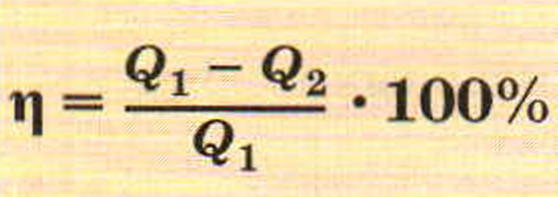

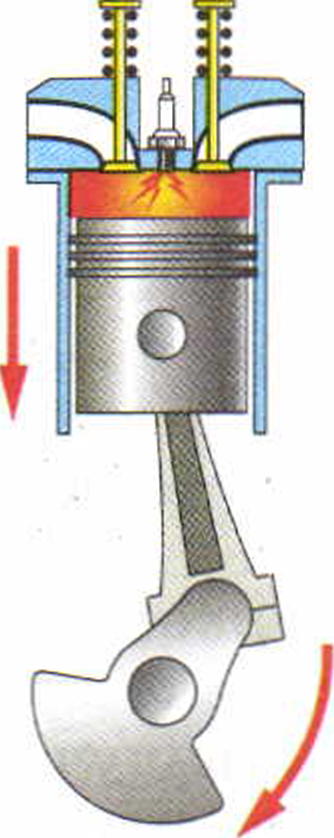
Рис. 29
Q1 - Q2 — количество теплоты, которое пошло на совершение работы. КПД выражается в процентах.
Например, двигатель из всей энергии, выделившейся при сгорании топлива, расходует на совершение полезной работы только одну четвёртую часть. Тогда коэффициент полезного действия двигателя равен 1/4 , или 25% .
КПД двигателя обычно выражают в процентах. Он всегда меньше единицы, т. е. меньше 100%. Например, КПД двигателей внутреннего сгорания 20—40%, паровых турбин — немногим выше 30%.

1. Почему в тепловых двигателях только часть энергии топлива превращается в механическую энергию? 2. Что называют КПД теплового двигателя? Почему КПД двигателя не может быть не только больше 100%, но и равен 100%? 4. Какой такт работы двигателя внутреннего сгорания изображён на рисунке 29?

Можно ли за счёт внутренней энергии тела, равной 200 Дж, совершить механическую работу в 200 Дж?
2. Тепловая машина за цикл получает от нагревателя количество теплоты, равное 155 Дж, а холодильнику отдаёт количество теплоты, равное 85 Дж. Определите КПД машины.
3. Определите количество теплоты, отданное двигателем внутреннего сгорания холодильнику, если его КПД равен 30%, а полезная работа равна 450 Дж.

Подготовьте доклад на одну из тем (по выбору).
История изобретения паровых машин.
История изобретения турбин.
Первые паровозы Стефенсона и Черепановых.
■ Достижения науки и техники в строительстве паровых турбин.
■ Использование энергии Солнца на Земле.
САМОЕ ГЛАВНОЕ
■ Температура является мерой средней кинетической энергии хаотического движения молекул.
■ Внутреннюю энергию тела можно изменить путём совершения работы или путём теплопередачи. Существует три способа теплопередачи: теплопроводность, конвекция, излучение.
■ Количеством теплоты называют энергию, которую тело получает или теряет в процессе теплопередачи.
■ Удельная теплоёмкость (с) — это физическая величина, которая показывает, какое количество теплоты необходимо затратить для нагревания 1 кг вещества на 1 град:
Q
с =-—-.
2 “ *i)
■ Количество теплоты, необходимое для нагревания тела или выделяемое им при охлаждении, рассчитывают по формуле:
Q = cm(t2 — t1); Q = cm At.
■ Удельная теплота сгорания топлива (q) — это физическая величина, которая показывает, какое количество теплоты выделяется при полном сгорании топлива массой 1 кг.
■ Количество теплоты, выделяемое при сгорании топлива, вычисляют по формуле: Q = qm.
■ Закон сохранения и превращения энергии: энергия не возникает и не исчезает, она только переходит из одного вида в другой, и значение её сохраняется.
■ Плавление — это переход вещества из твёрдого состояния в жидкое.
■ Кристаллизация (отвердевание) — это переход вещества из жидкого состояния в твёрдое.

■ Удельная теплота плавления (X) — это физическая величина, которая показывает, какое количество теплоты необходимо затратить для плавления 1 кг кристаллического вещества при температуре плавления.
■ Количество теплоты, необходимое для плавления кристаллического тела при температуре плавления, рассчитывают по формуле:
Q = Х/71.
■ Парообразование — это переход вещества из жидкого состояния в пар.
■ Испарение — это парообразование, происходящее с поверхности жидкости.
■ Конденсация — это превращение пара в жидкость.
■ Кипение — это процесс испарения жидкости, сопровождающийся образованием и ростом пузырьков пара по всему объёму жидкости, всплывающих на её поверхность при определённой температуре.
■ Температура кипения — это температура, при которой происходит кипение жидкости при нормальном давлении.
■ Удельная теплота парообразования (L) — это физическая величина, которая показывает, какое количество теплоты необходимо для обращения 1 кг жидкости в пар при постоянной температуре.
■ Количество теплоты, необходимое для превращения жидкости в пар, рассчитывают по формуле: Q = Lm.
■ Насыщенный пар — это пар, находящийся в динамическом равновесии со своей жидкостью.
■ Ненасыщенный пар — это пар, который не находится в состоянии равновесия со своей жидкостью.
■ Точкой росы называют температуру, при которой пар становится насыщенным (т. е. относительная влажность становится равной 100%) и дальнейшее понижение температуры приводит к конденсации водяного пара.
■ Тепловой двигатель — это машина, которая преобразует внутреннюю энергию топлива в механическую энергию.
КПД теплового двигателя определяют по формуле: 1] = ^ , или ц = £i^? .юо%.
1. К тепловым явлениям относятся:
A. движение Земли вокруг Солнца Б. падение мяча на землю
B. нагревание воды в чайнике
Г. притяжение магнитом иголки
2. Температура тела зависит от:
A. размеров тела
Б. скорости движения молекул
B. скорости движения тела
Г. положения тела относительно Земли
3. Книгу переместили с нижней полки на верхнюю, её внутренняя энергия:
A. изменилась
Б. не изменилась
B. превратилась в кинетическую
Г. книга не обладает внутренней энергией
4. Теплопередача — это:
A. изменение внутренней энергии при совершении работы над телом
Б. изменение внутренней энергии при совершении работы самим телом
B. изменение внутренней энергии без совершения работы над телом или самим телом
Г. явление передачи внутренней энергии от одной части тела к другой

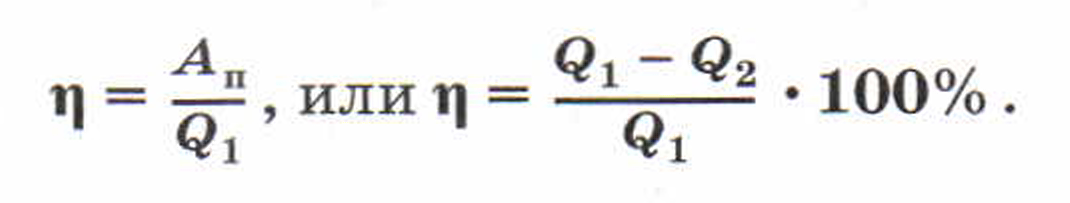
5. Установите соответствие между физическими величинами и единицами их измерения.
A) количество теплоты 1)Дж/кг
Б) удельная теплоёмкость 2) Д?к
B) удельная теплота сгорания 3) ДжДкг • °С)
6. Агрегатное состояние вещества определяется:
A. только расположением молекул
Б. характером движения и взаимодействия молекул
B. расположением молекул, характером движения и взаимодействия молекул
7. Влажность воздуха характеризуется:
A. плотностью водяного пара, содержащегося в воздухе Б. температурой, при которой пар, находящийся в воздухе, становится насыщенным
B. температурой, при которой жидкость начинает кипеть Г. температурой, при которой тело начинает плавиться
8. Установите соответствие между физическими величинами и их обозначением.
A) удельная теплота плавления 1) ср
Б) относительная влажность воздуха 2) X
B) удельная теплота парообразования 3) г|
Г) коэффициент полезного действия 4) L
9. КПД теплового двигателя может быть:
A. больше 100%
Б. равен 100%
B. меньше 100%
Г. всегда 50%
1. Выполните задания, предложенные в электронном приложении.
2. На сайте http://class-fizika.narod.ru найдите тесты по теме «Тепловые явления» и проверьте себя.
3. На сайте http://class-fizika.narod.ru найдите тесты по теме «Изменение агрегатных состояний вещества» и проверьте себя.

§1 Тепловое движение. Температура................................... 3
§ 2 Внутренняя энергия .................................................. 5
§ 3 Способы изменения внутренней энергии тела..................... 8
§4 Теплопроводность..................................................... 11
§ 5 Конвекция ............................................................. 14
ЭТО ЛЮБОПЫТНО...
Примеры конвекции в природе и технике................................ 17
§6 Излучение.............................................................. 18
ЭТО ЛЮБОПЫТНО...
Термос............................................................... 20
Теплопередача и растительный мир..................................... 21
§7 Количество теплоты. Единицы количества теплоты ............. 21
§ 8 Удельная теплоёмкость .............................................. 24
§ 9 Расчёт количества теплоты, необходимого для нагревания тела или выделяемого им при охлаждении........... 26
§ 10 Энергия топлива. Удельная теплота сгорания .................... 30
§ 11 Закон сохранения и превращения энергии в механических и тепловых процессах ............................................ 32
ЭТО ЛЮБОПЫТНО...
Использование энергии Солнца на Земле.................................. 35
§ 12 Агрегатные состояния вещества .................................... 36
§ 13 Плавление и отвердевание кристаллических тел................. 38
§ 14 График плавления и отвердевания кристаллических тел .......40
ЭТО ЛЮБОПЫТНО...
Аморфные тела. Плавление аморфных тел.................................. 42
§ 15 Удельная теплота плавления ........................................ 43
§ 16 Испарение. Насыщенный и ненасыщенный пар.................. 47
§ 17 Поглощение энергии при испарении жидкости и выделение её при конденсации пара.............................. 51
§ 18 Кипение ................................................................ 53
§ 19 Влажность воздуха. Способы определения влажности воздуха ................................................................. 56
§ 20 Удельная теплота парообразования и конденсации .............. 60
§ 21 Работа газа и пара при расширении ................................ 63
§ 22 Двигатель внутреннего сгорания.................................... 64
§ 23 Паровая турбина....................................................... 68
§ 24 КПД теплового двигателя ............................................ 69
ИТОГИ ГЛАВЫ............................................................. 71

§ 25 Электризация тел при соприкосновении. Взаимодействие заряженных тел ................................... 75
§26 Электроскоп............................................................ 78
§ 27 Электрическое поле ................................................... 80
§ 28 Делимость электрического заряда. Электрон ..................... 82
§ 29 Строение атомов ....................................................... 85
§ 30 Объяснение электрических явлений ............................... 87
§31 Проводники, полупроводники и непроводники электричества 90
ЭТО ЛЮБОПЫТНО...
Полупроводники........................................................... 93
§ 32 Электрический ток. Источники электрического тока............ 95
§ 33 Электрическая цепь и её составные части ......................... 99
§ 34 Электрический ток в металлах ...................................... 101
§ 35 Действия электрического тока ...................................... 103
§ 36 Направление электрического тока.................................. 106
§ 37 Сила тока. Единицы силы тока...................................... 107
§ 38 Амперметр. Измерение силы тока .................................. 110
§ 39 Электрическое напряжение.......................................... 112
§ 40 Единицы напряжения ................................................ 115
§ 41 Вольтметр. Измерение напряжения................................ 117
§ 42 Зависимость силы тока от напряжения ............................ 119
§ 43 Электрическое сопротивление проводников. Единицы сопротивления ............................................. 121
§ 44 Закон Ома для участка цепи ......................................... 123
§ 45 Расчёт сопротивления проводника. Удельное сопротивление .. 127
§ 46 Примеры на расчёт сопротивления проводника, силы тока и напряжения.......................................................... 131
§ 47 Реостаты................................................................ 133
§ 48 Последовательное соединение проводников....................... 135
§ 49 Параллельное соединение проводников............................ 138
§ 50 Работа электрического тока.......................................... 143
§ 51 Мощность электрического тока ..................................... 145
§ 52 Единицы работы электрического тока, применяемые на практике ........................................... 147
§ 53 Нагревание проводников электрическим током. Закон Джоуля—Ленца ............................................... 149
§ 54 Конденсатор............................................................ 151
§ 55 Лампа накаливания. Электрические нагревательные приборы................................................................. 156
§ 56 Короткое замыкание. Предохранители ............................ 159
ИТОГИ ГЛАВЫ............................................................. 161

§ 57 Магнитное поле........................................................ 165
§ 58 Магнитное поле прямого тока. Магнитные линии................ 167
§ 59 Магнитное поле катушки с током. Электромагниты и их применение....................................................... 169
§ 60 Постоянные магниты. Магнитное поле постоянных магнитов................................................................ 173
§ 61 Магнитное поле Земли................................................ 176
ЭТО ЛЮБОПЫТНО...
Зачем нужно магнитное поле планетам..................................... 179
§ 62 Действие магнитного поля на проводник с током. Электрический двигатель............................................ 180
ИТОГИ ГЛАВЫ............................................................. 185

§ 63 Источники света. Распространение света.......................... 187
§ 64 Видимое движение светил............................................ 192
§ 65 Отражение света. Закон отражения света ......................... 195
§ 66 Плоское зеркало....................................................... 198
ЭТО ЛЮБОПЫТНО...
Как Архимед поджёг римский флот......................................... 201
§ 67 Преломление света. Закон преломления света.................... 202
§ 68 Линзы. Оптическая сила линзы..................................... 206
§ 69 Изображения, даваемые линзой .................................... 209
§ 70 Глаз и зрение........................................................... 213
ЭТО ЛЮБОПЫТНО...
Близорукость и дальнозоркость. Очки................................... 215
ИТОГИ ГЛАВЫ............................................................. 217
ЛАБОРАТОРНЫЕ РАБОТЫ............................................................. 220
ОТВЕТЫ К УПРАЖНЕНИЯМ........................................................... 232
ПРЕДМЕТНО-ИМЕННОЙ УКАЗАТЕЛЬ .................................................. 233